Humira 20 mg oldatos injekció előretöltött fecskendőben
adalimumab
Mielőtt gyermeke elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára fontos információkat tartalmaz.
-
Tartsa meg a betegtájékoztatót, mert a benne szereplő információkra a későbbiekben is szüksége lehet.
-
Orvosától egy Betegkészenléti Kártyát is fog kapni fontos biztonsági információkkal, amit gyermekénél a Humira alkalmazása előtt és a Humira-val történő kezelés során is figyelembe kell venni. Tartsa magánál vagy gyermekénél ezt a Betegkészenléti Kártyát.
-
További kérdéseivel forduljon kezelőorvosához vagy gyógyszerészéhez.
-
Ezt a gyógyszert az orvos kizárólag az Ön gyermekének írta fel. Ne adja át a készítményt másnak, mert számára ártalmas lehet még abban az esetben is, ha a betegsége tünetei az Ön gyermekénél jelentkezőkhöz hasonlóak.
-
Ha gyermekénél bármilyen mellékhatás jelentkezik, tájékoztassa erről gyermeke kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik (lásd 4. pont).
A betegtájékoztató tartalma:
-
Milyen típusú gyógyszer a Humira és milyen betegségek esetén alkalmazható?
-
Tudnivalók a Humira alkalmazása előtt
-
Hogyan kell alkalmazni a Humira-t?
-
Lehetséges mellékhatások
-
Hogyan kell a Humira-t tárolni?
-
A csomagolás tartalma és egyéb információk
-
Használati utasítás
-
Milyen típusú gyógyszer a Humira és milyen betegségek esetén alkalmazható?
A Humira hatóanyaga az adalimumab.
A Humira az alábbi gyulladásos betegségek kezelésére alkalmazható:
-
Gyermekkori ismeretlen eredetű sokízületi gyulladás (poliartikuláris juvenilis idiopátiás artritisz)
-
Az inak tapadási helyének gyulladásos elváltozásával társult reumás ízületi gyulladás (entezitisszel társult artritisz)
-
Gyermekkori plakkos pszoriázis
-
A bélfal minden rétegére kiterjedő, nem fertőzéses eredetű gyulladás (gyermekkori Crohn-betegség)
-
Gyermekkori nem fertőzéses eredetű szemgyulladás (uveitisz)
A Humira hatóanyaga, az adalimumab egy emberi monoklonális antitest (ellenanyag). A monoklonális antitestek fehérjék, amelyek speciális célponthoz kötődnek.
Az adalimumab célpontja a tumor nekrózis faktor (TNF?) nevű fehérje, mely az immun (védekező) rendszer működésében vesz részt, és a fent felsorolt gyulladásos betegségekben megnövekedett mennyiségben van jelen. A TNF?-hoz való kötődéssel a Humira csökkenti ezen betegségek gyulladásos folyamatait.
Poliartikuláris juvenilis idiopátiás artritisz
A gyermekkori ismeretlen eredetű sokízületi gyulladás az ízületek gyulladásos betegsége, mely rendszerint elsőként gyerekkorban jelentkezik.
A Humira 2 éves kortól alkalmazható a gyermekkori ismeretlen eredetű sokízületi gyulladás (poliartikuláris juvenilis idiopátiás artritisz) kezelésére. A betegek először egyéb betegséget módosító gyógyszereket (pl. metotrexátot) kaphatnak. Ha ezek a gyógyszerek nem hatnak megfelelően, akkor fognak a betegek a poliartikuláris juvenilis idiopátiás artritisz kezelésére Humira-t kapni.
Kezelőorvosa fogja eldönteni, hogy a Humira-t metotrexáttal együtt, vagy önmagában alkalmazza. Entezitisszel társult artritisz
Az entezitisszel társult artritisz az inak tapadási helyének gyulladásos elváltozásával társult reumás ízületi gyulladás.
A Humira 6 éves kortól alkalmazható az entezitisszel társult artritisz kezelésére. A betegek először egyéb betegséget módosító gyógyszereket (pl. metotrexátot) kaphatnak. Ha ezek a gyógyszerek nem hatnak megfelelően, akkor fognak a betegek az entezitisszel társult artritisz kezelésre Humira-t kapni.
Gyermekkori plakkos pszoriázis (pikkelysömör)
A plakkos pszoriázis egy bőrbetegség, ami ezüstös pikkelyekkel borított piros, hámló, kérges foltokat okoz a bőrön. A plakkos pszoriázis a körmöket is érintheti, a köröm töredezését, megvastagodását, a körömágytól való elválását okozva, ami fájdalmas lehet. A pszoriázist vélhetően a szervezet immunrendszerének hibája okozza, amely a bőrsejtek fokozott termelődéséhez vezet.
A Humira alkalmazható súlyos, idült plakkos pszoriázis kezelésére 4-17 év közötti gyermekeknél, akiknél a helyi kezelés és a fényterápiák nem használtak, vagy nem alkalmazhatóak.
Gyermekkori Crohn-betegség
A Crohn-betegség az emésztőcsatorna gyulladásos kórfolyamata.
A Humira alkalmazható közepesen súlyos – súlyos Crohn-betegségben szenvedő, 6-17 éves korú gyermekek és serdülők kezelésére.
A betegek először egyéb gyógyszereket kaphatnak. Ha ezek a gyógyszerek nem hatnak megfelelően, akkor fognak a betegek a betegség jeleinek és tüneteinek enyhítésére Humira-t kapni.
Gyermekkori, nem fertőzéses eredetű szemgyulladás (uveitisz)
A nem fertőzéses eredetű szemgyulladás egy gyulladásos betegség, mely a szem bizonyos részeit érinti.
A Humira alkalmazható 2 éves kortól krónikus, nem fertőzéses eredetű uveitis kezelésére, amikor a gyulladás a szem elülső részét érinti.
A gyulladás látáscsökkenéshez és/vagy a szemben úszkáló homályok (fekete pontok vagy vékony csíkok, melyek a látótéren mozognak) jelenlétéhez vezethet. A Humira ezt a gyulladást csökkenti.
A betegek először egyéb gyógyszereket kaphatnak. Ha ezek a gyógyszerek nem hatnak megfelelően, akkor fognak a betegek a betegség jeleinek és tüneteinek enyhítésére Humira-t kapni.
-
Tudnivalók a Humira-nak az Ön gyermekénél történő alkalmazása előtt Ne alkalmazza a Humira-t
Ha gyermeke allergiás az adalimumabra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Ha gyermeke súlyos fertőzésben szenved, beleértve az aktív tuberkulózist (lásd
„Figyelmeztetések és óvintézkedések”). Kezelőorvosával feltétlenül közölje, ha gyermekének bármilyen fertőzésre utaló tünete van, mint pl. láz, sebek, fáradtságérzés, fogászati problémák.
Ha gyermeke középsúlyos vagy súlyos szívelégtelenségben szenved. Kezelőorvosával feltétlenül közölje, ha gyermekének súlyos szív problémája van vagy volt (lásd
„Figyelmeztetések és óvintézkedések”).
Figyelmeztetések és óvintézkedések
A Humira alkalmazása előtt beszéljen gyermeke kezelőorvosával vagy gyógyszerészével. Allergiás reakciók:
Ha gyermeke allergiás reakciót észlel olyan tünetekkel, mint a mellkasi szorítás, asztmás légzés, szédülés, duzzanat vagy kiütés, ne alkalmazza a Humira-t és azonnal forduljon orvosához.
Fertőzések:
Ha gyermeke fertőzésben szenved, beleértve a hosszantartó vagy helyi fertőzést is (pl. lábszárfekély), a Humira alkalmazása előtt beszéljen orvosával. Ha kétségei vannak, forduljon orvosához.
Humira-kezelés során gyermeke könnyebben kaphat meg fertőzéseket. Ennek veszélye nagyobb lehet, ha a légzésfunkciója károsodott. Ezek a fertőzések súlyosak lehetnek és közéjük tartozik
-
a tuberkulózis
-
a vírusok, gombák, élősködők vagy baktériumok okozta fertőzések
-
súlyos vérfertőzés (szepszis)
Ritka esetekben ezek a reakciók életveszélyesek lehetnek. Fontos, hogy közölje kezelőorvosával, ha gyermekének olyan tünete van, mint a láz, sebek, fáradtságérzés, fogászati problémák. Orvosa a Humira-kezelés átmeneti felfüggesztését javasolhatja.
Tájékoztassa kezelőorvosát, ha gyermeke olyan területen él vagy olyan területre utazik, ahol a gombák okozta fertőzések, (mint például a hisztoplazmózis, kokcidioidomikózis vagy a blasztomikózis) nagyon gyakoriak.
Közölje orvosával, ha gyermeke kórelőzményében visszatérő fertőzés szerepel, vagy egyéb olyan állapot áll fenn, ami a fertőzés lehetőségét fokozza.
Gyermekének és kezelőorvosának kiemelt figyelmet kell fordítania a fertőzés jeleire a Humira-kezelés során. Fontos, hogy mondja el gyermeke kezelőorvosának, ha gyermekének
fertőzésre utaló tünetei vannak, mint például láz, sebek, fáradtságérzés vagy fogászati problémák.
Tuberkulózis
-
Mivel Humira-val kezelt betegeken tuberkulózis kialakulását észlelték, így a Humira-kezelés megkezdése előtt kezelőorvosa az Ön gyermekénél megvizsgálja a
tuberkulózisra utaló jeleket és tüneteket. Ebbe beletartozik gyermeke részletes orvosi kórelőzményének elemzése és a megfelelő szűrővizsgálatok (mint pl. mellkasröntgen vizsgálatra és tuberkulin teszt) elvégzése. Gyermeke Betegkészenléti Kártyáján a vizsgálatok elvégzésének tényét és eredményét vezetni kell.
-
Nagyon fontos, hogy közölje kezelőorvosával, ha gyermeke bármikor tuberkulózisban szenvedett vagy közeli kapcsolatban volt bárkivel, akinek tuberkulózisa volt. Ha gyermekének aktív tuberkulózisa van, ne használja a Humira-t.
-
A tuberkulózis kialakulhat a kezelés során annak ellenére is, hogy gyermekénél tuberkulózis elleni megelőző terápiát alkalmaztak.
-
Ha a tuberkulózis tünetei (mint például hosszan tartó köhögés, testsúlycsökkenés, erőtlenség, hőemelkedés), vagy más fertőzésre utaló tünetek jelentkeznek a kezelés alatt vagy a kezelést követően, azonnal közölje orvosával.
Hepatitis B
Figyelmeztesse orvosát arra, ha gyermeke hepatitisz B vírus (HBV) -hordozó, netán aktív HBV fertőzésben szenved, vagy feltételezi, hogy hepatitisz B fertőzés veszélye fenyegetheti.
-
Gyermeke orvosának HBV-vizsgálatot kell végeznie gyermekénél. A Humira a vírushordozókban ismét aktiválhatja a HBV-t.
-
Egyes ritka esetekben – különösen ha gyermeke más, az immunrendszer működését gátló szereket is szed – a HBV ismételt aktiválódása életveszélyes lehet.
Sebészeti vagy fogászati beavatkozás:
Ha gyermeke sebészeti vagy fogászati beavatkozás előtt áll, tájékoztassa orvosát, hogy Humira- kezelésben részesül. Orvosa a kezelés átmeneti felfüggesztését javasolhatja.
Demielinizációval járó betegség
Ha gyermeke demielinizációval (az idegrostok velőshüvelyét érintő betegség, mint például szklerózis multiplex) járó betegségben szenved vagy ilyen típusú betegség alakul ki nála, kezelőorvosa dönti el, hogy a Humira-kezelés alkalmazható-e, vagy folytatható-e gyermeke esetében. Azonnal tájékoztassa kezelőorvosát, ha gyermeke olyan tüneteket tapasztal, mint a megváltozott látás, kar- vagy lábgyengeség, illetve zsibbadás vagy bizsergés a test bármelyik részén.
Védőoltások
Bizonyos védőoltások fertőzést okozhatnak, és ezért nem adhatóak a Humira-kezelés során.
-
Védőoltás gyermekének történő beadását megelőzően beszéljen orvosával.
-
Ajánlott, hogy a gyermekek– ha lehetséges-a Humira kezelés megkezdése előtt minden, az életkoruknak megfelelően ütemezett védőoltást kapjanak meg.
-
Ha a terhessége alatt Humira-t kapott, a kisbabája a terhesség alatt kapott utolsó adagot követően legfeljebb 5 hónapig nagyobb eséllyel kaphat el valamilyen fertőzést. Fontos, hogy elmondja kisbabája orvosának vagy az őt kezelő egészségügyi személyzetnek, hogy a terhessége alatt Humira-t kapott, így ők el tudják dönteni, hogy kisbabájának mikor kell valamilyen védőoltást kapnia.
Szívelégtelenség
Ha gyermekének enyhe szívelégtelensége van és Humira-kezelést kap, szívelégtelenség állapotát orvosának szorosan követnie kell. Fontos, hogy közölje kezelőorvosával, ha gyermekének súlyos szívbetegsége volt, vagy jelenleg is van. Ha új tünetek kialakulását vagy a szívelégtelenség tüneteinek rosszabbodását észleli (pl. légszomj, vagy lábdagadás), azonnal közölje orvosával. A kezelőorvos el fogja dönteni, hogy az Ön gyermeke kaphat-e Humira-t.
Láz, véraláfutás, vérzés vagy sápadtság
Egyes betegek esetében a szervezet nem termel elég olyan vérsejtet, melyek leküzdenék a fertőzést, vagy segítenének megállítani a vérzést. Kezelőorvosa dönthet úgy, hogy abbhagyják a kezelést. Ha gyermekének csillapíthatatlan láza van, véraláfutása van, vagy könnyen vérzik és sápadtnak látszik, azonnal értesítse orvosát.
Daganatos betegség
Nagyon ritkán előfordul, hogy a Humira-t vagy más TNF-antagonista gyógyszert szedő betegeknél bizonyos daganatfajta jelentkezik.
-
A hosszú ideje súlyos reumatoid artritiszben szenvedő betegeknek az átlagosnál nagyobb a kockázatuk, hogy limfóma (a nyirokrendszert érintő daganat) vagy leukémia (a vért és a csontszövetet érintő daganat) alakul ki.
-
Amennyiben gyermeke Humira-t kap, a limfóma, leukémia vagy egyéb daganat kialakulásának kockázata fokozódhat. Ritka esetekben a nyirokdaganat (limfóma) egy ritka és súlyos típusát észlelték Humira-val kezelt betegeknél. E betegek közül egyeseket egyidejűleg azatioprinnel, illetve 6-merkaptopurinnal is kezeltek.
-
Közölje orvosával, ha a gyermeke a Humira-val egyidejűleg azatioprint vagy 6- merkaptopurint szed.
-
Ezen kívül, esetenként nem melanomás bőrrák kialakulását észlelték Humira-val kezelt betegeken.
-
Ha új bőrelváltozások jelennek meg a kezelés alatt vagy a kezelést követően, vagy a meglévők külleme megváltozik, tájékoztassa kezelőorvosát.
Voltak esetek, amikor egy adott tüdőbetegségben (amelyet idült obstruktív tüdőbetegségnek (COPD-nek) neveznek) szenvedő, TNF-antagonistával kezelt betegeken nem limfóma természetű rákos daganatok kialakulását észlelték. Ha gyermeke COPD-ben szenved vagy erős dohányos, kérje orvosa tanácsát, hogy vajon a TNF-antagonistával végzett kezelés megfelelő-e gyermeke számára.
Autoimmun betegség
-
Ritka esetekben a Humira lupusz-szerű szindrómát okozhat. Keresse fel kezelőorvosát, ha olyan tüneteket észlel, mint a tartós, tisztázatlan eredetű kiütés, láz, ízületi fájdalom vagy fáradtság.
Egyéb gyógyszerek és a Humira
Feltétlenül tájékoztassa gyermeke kezelőorvosát vagy gyógyszerészét gyermeke jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.
Gyermeke nem kaphat Humira-t a következő hatóanyagot tartalmazó gyógyszerekkel együtt, mert fokozódik a súlyos fertőzések kockázata:
-
anakinra
-
abatacept.
A Humira-t lehet együtt alkalmazni:
-
metotrexáttal
-
egyes betegséget befolyásoló reumaellenes szerrel (mint például a szulfaszalazin, hidroxiklorokin, leflunomid és arany injekció)
-
szteroidokkal vagy fájdalomcsillapító készítményekkel, beleértve a nem szteroid gyulladáscsökkentőket (NSAID-ket).
Ha kérdése van, kérdezze meg kezelőorvosát.
Terhesség és szoptatás
A Humira alkalmazása terhesség nőknek nem javasolt. Gyermeke számára javasolt a terhesség megelőzése és megfelelő fogamzásgátlás alkalmazása a Humira-val történő kezelés során és a Humira-val történt utolsó kezelést követően legalább 5 hónapig. Amennyiben gyermeke teherbe esik, beszéljen kezelőorvosával.
Az adalimumab anyatejbe történő kiválasztása
Ha gyermeke szoptató anya, a szoptatást Humira-val történő kezelés során és a Humira-val történt utolsó kezelést követően legalább 5 hónapig abba kell hagynia.
Ha gyermeke úgy gondolja, hogy terhes lehet vagy gyermeket tervez, kérjen kezelőorvosától vagy gyógyszerészétől tamácsot, mielőtt gyermeke ezt a gyógyszert alkalmazza.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
A Humira csekély mértékben befolyásolhatja gyermeke gépjárművezetéshez, kerékpározáshoz vagy a gépek kezeléséhez szükséges képességeit. Előfordulhat olyan érzés, mintha forogna a szoba vagy a tér, továbbá látászavar is előfordulhat.
-
Hogyan kell alkalmazni a Humira-t?
A gyógyszert mindig a gyermeke kezelőorvosa vagy gyógyszerésze által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg gyermeke kezelőorvosát vagy gyógyszerészét.
A Humira ajánlott adagját az egyes engedélyezett javallatokban a következő táblázat tartalmazza. Kezelőorvosa más hatáserősségű Humira-t is felírhat, ha gyermekének más dózisra van szüksége.
|
Poliartikuláris juvenilis idiopátiás artritisz |
|
Kor vagy testtömeg |
Milyen adagot és milyen gyakran kell alkalmazni? |
Megjegyzés |
|
2 évesnél idősebb, 30 kg vagy annál nagyobb testtömegű gyermekek, serdülők és felnőttek |
40 mg minden második héten |
Nincs |
|
2 évesnél idősebb, 10 kg-nál nagyobb, de 30 kg-nál kisebb testtömegű gyermekek és serdülők |
20 mg minden második héten |
Nincs |
|
Entezitisszel társult artritisz |
|
Kor vagy testtömeg |
Milyen adagot és milyen gyakran kell alkalmazni? |
Megjegyzés |
|
6 évesnél idősebb, 30 kg vagy annál nagyobb testtömegű gyermekek, serdülők és felnőttek |
40 mg minden második héten |
Nincs |
|
6 évesnél idősebb, 15 kg-nál nagyobb, de 30 kg-nál kisebb testtömegű gyermekek és serdülők |
20 mg minden második héten |
Nincs |
|
Gyermekkori plakkos pszoriázis |
|
Kor vagy testtömeg |
Milyen adagot és milyen gyakran kell alkalmazni? |
Megjegyzés |
|
4-17 éves kor közötti, 30 kg vagy annál nagyobb testtömegű gyermekek és serdülők |
Első alkalommal 40 mg, majd egy héttel később 40 mg.
Ezt követően, a szokásos adag 40 mg minden második héten. |
Nincs |
|
4-17 éves kor közötti, 15 kg-nál nagyobb, de 30 kg-nál kisebb testtömegű gyermekek és serdülők |
Első alkalommal 20 mg, majd egy héttel később 20 mg.
Ezt követően, a szokásos adag 20 mg minden második héten. |
Nincs |
|
Gyermekkori Crohn-betegség |
|
Kor vagy testtömeg |
Milyen adagot és milyen gyakran kell alkalmazni? |
Megjegyzés |
|
6-17 éves kor közötti, 40 kg-os vagy annál nagyobb testtömegű gyermekek és serdülők |
Első alkalommal 80 mg, majd 2 héttel később 40 mg.
Amennyiben gyorsabb terápiás válaszra van szükség, gyermeke kezelőorvosa rendelhet 160 mg kezdő dózist, melyet 80 mg követ két héttel később.
Ezt követően, a szokásos adag 40 mg minden második héten. |
Gyermeke kezelőorvosa megemelheti az adagolás gyakoriságát heti 40 mg-ra. |
|
6-17 éves kor közötti, 40 kg-nál kisebb testtömegű gyermekek és serdülők |
Első alkalommal 40 mg, majd 2 héttel később 20 mg
Amennyiben gyorsabb terápiás válaszra van szükség, gyermeke kezelőorvosa rendelhet 80 mg kezdő dózist, melyet 40 mg követ két héttel később
Ezt követően, a szokásos adag 20 mg minden második héten. |
Gyermeke kezelőorvosa megemelheti az adagolás gyakoriságát heti 20 mg-ra. |
|
Gyermekkori nem fertőzéses eredetű szemgyulladás (uveitisz) |
|
Kor vagy testtömeg |
Milyen adagot és milyen gyakran kell alkalmazni? |
Megjegyzés |
|
2 éves kor feletti, 30 kg-nál kisebb testtömegű gyermekek és serdülők |
20 mg minden második héten |
Kezelőorvosa egy 40 mg-os kezdő dózist is felírhat, melyet egy héttel a szokásos, kéthetente 20 mg-os adagolás megkezdése előtt kell beadni. A Humira-t metotrexáttal kombinálva javasolt alkalmazni. |
|
2 éves kor feletti, 30 kg vagy annál nagyobb testtömegű gyermekek és serdülők |
40 mg minden második héten |
Kezelőorvosa egy 40 mg-os kezdő dózist is felírhat, melyet egy héttel a szokásos, kéthetente 40 mg-os adagolás megkezdése előtt kell beadni. A Humira-t metotrexáttal kombinálva javasolt alkalmazni. |
Az alkalmazással kapcsolatos tudnivalók és az alkalmazás módja
A Humira-t a bőr alá (szubkután injekció formájában) kell beadni.
A Humira injekció beadásával kapcsolatos részletes útmutatás a „7. Használati utasítás” című pontban található.
Ha az előírtnál több Humira-t alkalmazott:
Ha véletlenül a kezelőorvosa vagy gyógyszerésze által előírtnál gyakrabban alkalmazta a Humira-t, azonnal közölje ezt kezelőorvosával vagy gyógyszerészével. Őrizze meg a külső csomagolást vagy az üveget, abban az esetben is, ha üres.
Ha elfelejtette alkalmazni a Humira-t:
Ha elfelejtette beadni gyermekéknek az injekciót, adja be a következő Humira adagot rögtön, amikor eszébe jutott. A következő adagot az eredeti kezelési terv alapján meghatározott napon adja be gyermekének, úgy mintha az előző adagot az előírás szerinti időpontban adta volna be.
Ha idő előtt abbahagyja a Humira alkalmazását:
A döntést, hogy abbahagyja a Humira alkalmazását, meg kell beszélni kezelőorvosával. Gyermekének tünetei visszatérhetnek, ha abbahagyja a kezelést.
Ha bármilyen további kérdése van a készítmény alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
-
Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek. A legtöbb mellékhatás enyhe vagy közepes fokú. Néhány esetben kezelést igénylő, súlyos mellékhatás is előfordulhat. A mellékhatások az utolsó Humira injekciót követően legalább 4 hónapig még bekövetkezhetnek.
Közölje azonnal kezelőorvosával, ha az alábbiak közül bármit észlel:
súlyos kiütés, csalánkiütés vagy más allergiára utaló tünet;
duzzanat az arcon, kezeken vagy lábakon;
nehézlégzés vagy nehézség a nyelés során;
megerőltetéskor vagy lefekvéskor jelentkező nehézlégzés, vagy lábdagadás.
Közölje kezelőorvosával amint lehetséges, ha az alábbiak közül bármit észlel:
fertőzésre utaló tünet, mint láz, rossz közérzet, sebek, fogászati problémák, vizeléskor jelentkező égő érzés;
gyengeség vagy fáradtságérzés;
köhögés;
fülzúgás;
zsibbadás;
kettős látás;
kar vagy lábgyengeség;
duzzanat vagy nyílt fekély, amelyik nem gyógyul;
vérképzőszervi betegségre jellemző jelek és tünetek, mint állandó láz, véraláfutás, vérzés, sápadtság.
A fent leírt tünetek az alábbiakban felsorolt mellékhatások jelei is lehetnek, melyeket a Humira alkalmazása során észleltek:
Nagyon gyakori (10 beteg közül több mint 1-nél kialakuló)
helyi reakció az injekció beadásának helyén, (beleértve fájdalom, duzzadás, vörösség vagy viszketés);
légúti fertőzések (beleértve a megfázást, orrfolyást, melléküreg-gyulladást, tüdőgyulladást is);
fejfájás;
hasi fájdalom;
hányinger és hányás;
bőrkiütés;
mozgásszervi eredetű fájdalom.
Gyakori (10 beteg közül legfeljebb 1-nél kialakuló)
szisztémás fertőzések (beleértve a vérmérgezést és az influenzát is);
bélfertőzések (beleértve a gyomor-bélgyulladást);
bőrfertőzések (beleértve a kötőszövet-gyulladást és az övsömört is);
fülfertőzések;
szájüregi fertőzések (beleértve a fogfertőzéseket és az ajakherpeszt is);
a nemiszervek fertőzései;
húgyúti fertőzések;
gombás fertőzések;
ízületi fertőzések;
jóindulatú daganatok;
bőrrák;
allergiás reakciók (beleértve a szezonális allergiát is);
kiszáradás;
hangulatváltozás (beleértve a depressziót is);
szorongás;
álmatlanság;
érzészavarok, például bizsergés, szurkáló érzés vagy zsibbadás;
migrén;
ideggyök nyomási tünetei (beleértve a derékfájdalmat és a lábfájást is);
látászavar;
szemgyulladás;
a szemhéj gyulladása és a szem duzzanata;
forgó jellegű szédülés;
gyors szívverés-érzés;
magas vérnyomás;
kipirulás;
vérömleny;
köhögés;
asztma;
légszomj;
tápcsatorna eredetű vérzés;
diszpepszia (emésztési zavar, puffadás, gyomorégés);
a gyomorsav visszafolyása a nyelőcsőbe;
szikka-szindróma (beleértve a száraz szemet és a száraz szájat is);
bőrviszketés;
viszkető bőrkiütés;
véraláfutás;
bőrgyulladás (mint például az ekcéma);
a kéz- és lábujjkörmök töredezése;
fokozott verejtékezés;
hajhullás;
pikkelysömör megjelenése vagy rosszabbodása;
izomgörcsök;
véres vizelet;
veseproblémák;
mellkasi fájdalom;
vizenyő;
láz;
a vérlemezkék számának csökkenése, ami növeli a vérzés vagy a véraláfutás kialakulásának kockázatát;
csökkent gyógyulási készség.
Nem gyakori (100 beteg közül legfeljebb 1-nél kialakuló)
opportunista fertőzések (ezek közé tartozik a tuberkulózis és más, olyan fertőzések, amelyek akkor alakulnak ki, amikor a betegségekkel szembeni ellenállóképesség lecsökken);
ideggyógyászati eredetű fertőzések (beleértve a vírusos eredetű agyhártyagyulladást is);
szemfertőzések;
baktériumok okozta fertőzések;
divertikulitisz (vastagbélgyulladás és -fertőzés);
rák;
rák, amely a nyirokrendszert támadja meg;
melanóma;
a szervezet védekező rendszerének betegségei, amelyek érinthetik a tüdőt, a bőrt és a nyirokcsomókat (leggyakrabban szarkoidózisként jelentkezik);
vaszkulitisz (érgyulladás);
tremor (remegés);
érzékzavar;
szélütés
halláscsökkenés, fülzúgás;
szabálytalan szívverés érzése, mint például kimaradó szívverés;
szívproblémák, amelyek például nehézlégzést vagy bokadagadást okozhatnak;
szívroham;
kiöblösödés valamely nagy ütőérben, gyulladás és vérrögképződés valamelyik vénában, érelzáródás;
nehézlégzést okozó tüdőbetegségek (beleértve a gyulladást is);
tüdőembólia (a tüdőt ellátó ér elzáródása);
pleurális folyadékgyülem (a mellhártyák között kóros folyadékgyülem);
hasnyálmirigy-gyulladás ami erős hasi fájdalmat és hátfájást okoz;
nyelészavar;
az arc feldagadása;
epehólyaggyulladás, epekövesség;
zsírmáj;
éjszakai izzadás;
hegképződés;
az izomszövet kóros szétesése;
szisztémás lupusz eritematózusz (beleértve a bőr, a szív, a tüdő, az ízületek és más szervrendszerek gyulladását);
az alvás megszakadása;
merevedési zavar;
gyulladások.
Ritka (1000 beteg közül legfeljebb 1-nél kialakuló)
leukémia (fehérvérűség, a vérképző rendszer daganata, ami a csontvelőt érinti);
súlyos, sokkot okozó allergiás reakció;
szklerózis multiplex;
ideggyógyászati betegségek (pl. a látóideg gyulladása vagy Guillain-Barré-szindróma, ami izomgyengeséget, érzészavart, a karok és a felsőtest zsibbadását okozhatja);
szívleállás;
tüdőfibrózis (tüdőhegesedés);
bél átlyukadása;
májgyulladás;
B típusú fertőző májgyulladás kiújulása;
autoimmun májgyulladás (a máj gyulladása, melyet a saját immunrendszer vált ki);
kután vaszkulitisz (a bőrben található erek gyulladása);
Stevens-Johnson-szindróma (korai tünetei a rossz közérzet, láz, fejfájás és bőrkiütés);
arcduzzanat, amit allergiás reakció kísér;
eritéma multiforme (gyulladásos bőrkiütés);
lupusz-szerű szindróma;
angioödéma (helyi bőrduzzanat).
Nem ismert (a rendelkezésre álló adatokból nem állapítható meg)
hepatoszplénikus T-sejtes limfóma (ritka vérrák, ami gyakran halálos kimenetelű);
Merkel-sejtes karcinóma (bőrrák egyik típusa);
májelégtelenség;
dermatomiozitisz nevű betegség (izomgyengeséghez társult bőrkiütés formájában jelentkezik) súlyosbodása.
A Humira alkalmazása során észlelt némelyik mellékhatás nem okoz tüneteket, és lehet, hogy csak vérvizsgálattal deríthető ki. Ezek közé tartozik:
Nagyon gyakori (10 beteg közül több mint 1-nél alakul ki)
alacsony fehérvérsejtszám;
alacsony vörösvértestszám;
a vérzsírszint emelkedése;
emelkedett májenzimszint.
Gyakori (10 ember közül legfeljebb 1-nél alakul ki)
magas fehérvérsejtszám;
alacsony vérlemezkeszám;
emelkedett húgysavszint a vérben;
kóros nátriumszint a vérben;
alacsony kalciumszint a vérben;
alacsony foszfátszint a vérben;
magas vércukorszint;
emelkedett laktát-dehidrogenáz-szint a vérben;
autoantitestek megjelenése a vérben;
alacsony káliumszint a vérben.
Nem gyakori (100 beteg közül legfeljebb 1-nél alakul ki)
Ritka (1000 beteg közül legfeljebb 1-nél alakul ki)
alacsony fehérvérsejtszám, vörösvértestszám és vérlemezkeszám.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik.
A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
-
Hogyan kell a Humira-t tárolni?
A gyógyszer gyermekektől elzárva tartandó.
A címkén/buborékcsomagoláson/kartondobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert.
Hűtőszekrényben (2°C-8?C) tárolandó. Nem fagyasztható!
A fénytől való védelem érdekében az előretöltött injekciós toll az eredeti dobozban tárolandó. További tárolási lehetőség:
Amennyiben szükséges (pl. utazás alatt), úgy önmagában a Humira előretöltött injekciós toll legfeljebb 25?C-on, maximum 14 napig tárolható. A fénytől való védelmet biztosítani kell. Ha a hűtőgépből kivette, hogy szobahőmérsékleten tartsa, úgy a fecskendőt 14 napon belül fel kell használni, vagy meg kell semmisíteni, még akkor is, ha visszatette a hűtőszekrénybe.
Jegyezze fel, hogy mikor vette ki először a fecskendőt a hűtőszekrényből, és azt a dátumot is, ami után azt meg kell semmisíteni.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
-
A csomagolás tartalma és egyéb információk Mit tartalmaz a Humira?
A készítmény hatóanyaga: adalimumab.
Egyéb összetevők: mannit, poliszorbát 80 és injekcióhoz való víz.
Milyen a Humira előretöltött injekciós fecskendő külleme és mit tartalmaz a csomagolás?
A Humira 20 mg oldatos injekció előretöltött fecskendőben 20 mg adalimumabot tartalmazó 0,2 ml steril oldat formájában kerül forgalomba.
A Humira előretöltött fecskendő egy adalimumab oldatot tartalmazó üveg fecskendő.
A Humira előretöltött fecskendő 2 db előretöltött fecskendőt és 2 db alkoholos törlőkendőt tartalmazó csomagban kerül forgalomba.
A Humira injekciós üvegben, előretöltött fecskendőben és előretöltött injekciós tollban kapható.
A forgalomba hozatali engedély jogosultja
AbbVie Ltd Maidenhead SL6 4UB
Nagy-Britannia
Gyártó
AbbVie Biotechnology GmbH Max-Planck-Ring 2
D-65205 Wiesbaden Németország
és
AbbVie Biotechnology GmbH Knollstrasse
67061 Ludwigshafen Németország
A készítményhez kapcsolódó további kérdéseivel forduljon a forgalomba hozatali engedély jogosultjának helyi képviseletéhez:
België/Belgique/Belgien
AbbVie SA
Tél/Tel: +32 10 477811
????????
???? ???? ???.:+359 2 90 30 430
Česká republika
AbbVie s.r.o.
Tel: +420 233 098 111
Danmark
AbbVie A/S
Tlf: +45 72 30-20-28
Deutschland
AbbVie Deutschland GmbH & Co. KG Tel: 00800 222843 33 (gebührenfrei)
Tel: +49 (0) 611 / 1720-0
Eesti
AbbVie Biopharmaceuticals GmbH Eesti filiaal Tel: +372 623 1011
??????
AbbVie ???????????? ?.?. ???: +30 214 4165 555
Espana
AbbVie Spain, S.L.U. Tel: +34 9 1 384 09 10
France
AbbVie
Tél: +33 (0) 1 45 60 13 00
Hrvatska
AbbVie d.o.o.
Tel + 385 (0)1 5625 501
Ireland
AbbVie Limited
Tel: +353 (0)1 4287900
Ísland
Vistor hf.
Tel: +354 535 7000
Lietuva
AbbVie UAB
Tel: +370 5 205 3023
Luxembourg/Luxemburg AbbVie SA Belgique/Belgien
Tél/Tel: +32 10 477811
Magyarország
AbbVie Kft. Tel.:+36 1 455 8600
Malta
V.J.Salomone Pharma Limited Tel: +356 22983201
Nederland
AbbVie B.V.
Tel: +31 (0)88 322 2843
Norge
AbbVie AS
Tlf: +47 67 81 80 00
Österreich AbbVie GmbH Tel: +43 1 20589-0
Polska
AbbVie Polska Sp. z o.o. Tel.: +48 22 372 78 00
Portugal
AbbVie, Lda.
Tel: +351 (0)21 1908400
România
AbbVie S.R.L.
Tel: +40 21 529 30 35
Slovenija
AbbVie Biofarmacevtska družba d.o.o. Tel: +386 (1)32 08 060
Slovenská republika
AbbVie s.r.o.
Tel: +421 2 5050 0777
Italia
AbbVie S.r.l.
Tel: +39 06 928921
??????
Lifepharma (Z.A.M.) Ltd ???.: +357 22 34 74 40
Latvija
AbbVie SIA
Tel: +371 67605000
Suomi/Finland
AbbVie Oy
Puh/Tel: +358 (0)10 2411 200
Sverige
AbbVie AB
Tel: +46 (0)8 684 44 600
United Kingdom
AbbVie Ltd
Tel: +44 (0)1628 561090
A betegtájékoztató legutóbbi felülvizsgálatának dátuma:
A gyógyszerről részletes információ az Európai Gyógyszerügynökség internetes honlapján (http://www.ema.europa.eu/) található.
A betegtájékoztató meghallgatásának, <Braille írással>, <nagyméretű betűkkel> készült vagy
<audio> változatának igénylése érdekében forduljon a forgalomba hozatali engedély jogosultjának helyi képviselőjéhez.
-
Használati utasítás
-
A következő útmutató azt magyarázza el, hogyan adja be gyermekének a bőre alá a Humira injekciót előretöltött fecskendővel. Kérjük, figyelmesen olvassa el az útmutatót, és kövesse lépésről-lépésre.
-
Az injekciózás technikájára kezelőorvosa, a nővér, vagy gyógyszerésze tanítja meg Önt.
-
Ne próbálkozzon az gyermeke injekciózásával, amíg nem biztos abban, hogyan kell elkészíteni és beadni az injekciót.
-
Megfelelő gyakorlás után Ön vagy más személy (pl. családtag, ismerős) is beadhatja gyermekének az injekciót.
-
Minden egyes előretöltött fecskendőt csak egyszeri beadásra használja!
Humira előretöltött fecskendő
dugattyú ujjtámasz tűvédő tok
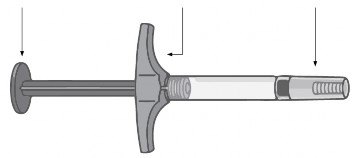
Ne használja az előretöltött fecskendőt és hívja kezelőorvosát vagy gyógyszerészét, ha:
-
a folyadék zavaros, elszíneződött vagy pelyhes csapadékot vagy lebegő részecskéket tartalmaz
-
a lejárati idő (EXP) elmúlt
-
a folyadék megfagyott vagy közvetlen napfénynek volt kitéve
-
az előretöltött fecskendő leesett vagy eltörött
A tűvédő tokot ne távolítsa el, csak közvetlenül az injekció beadása előtt. A Humira gyermekektől elzárva tartandó!
|
Vegye ki a Humira-t a hűtőszekrényből.
A beadás előtt 15-30 percig hagyja a Humira-t szobahőmérsékleten.
|
|
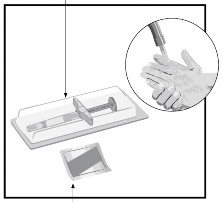
2. lépés
Előretöltött fecskendő
Törlőkendő |
Ellenőrizze a lejárat dátumát (EXP). Ne használja az előretöltött fecskendőt, ha a lejárati idő (EXP) elmúlt.
Helyezze a következőket egy tiszta, sima felületre:
Mossa meg és szárítsa meg a kezét. |
|
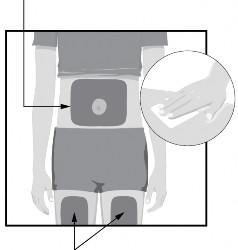
3. lépés Beadási helyek
Beadási helyek |
Válassza ki a beadási helyet:
Körkörös mozdulattal törölje le az injekció beadásának helyét az alkoholos törlővel.
|
|
4. lépés |
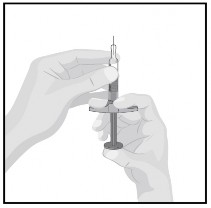
Tartsa az előretöltött fecskendőt az egyik kezében. Ellenőrizze a folyadékot az előretöltött fecskendőben. |
-
lépés
-
Ne távolítsa el a tűvédő tokot, amíg a Humira hőmérséklete eléri a szobahőmérsékeletet.
-
Ne melegítse a Humira-t semmilyen egyéb módon. Például ne melegítse mikrohullámú sütőben vagy forró vízben.
-
Gyermeke combjának elülső részén vagy
-
Gyermeke hasfalán, legalább 5 cm távolságra a köldökétől
-
Az előző beadási helytől legalább 3 cm távolságra
-
Ne ruhán keresztül adja be az injekciót
-
Ne adja az injekciót olyan helyre, ahol a bőr sebes, véraláfutásos, bepirosodott, kemény, heges, a bőr megnyúlását jelző világos csíkok (striák) területén, illetve a pikkelysömörös területeken
-
Bizonyosodjon meg róla, hogy a folyadék tiszta és színtelen
-
Ne használja az előretöltött fecskendőt, ha a folyadék zavaros vagy részecskéket tartalmaz

|
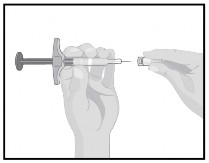
Óvatosan húzza le a tűvédő tokot a másik kezével. Dobja ki a tokot. Ne rakja vissza.
|
|
5. lépés |
Tartsa az előretöltött fecskendőt a tűvel felfelé.
Lassan nyomja be a dugattyút, hogy a levegőt kijöjjön a tűből.
|
|
6. lépés |
|
|
|
Tartsa egy kézzel az előretöltött fecskendőt a közepénél, a |
|
|
hüvelyk- és mutatóujja között, mintha egy ceruzát fogna. |
|
|
A beadás helyén szorítsa össze a gyermeke bőrét egy |
|
|
kiemelkedő redőbe, és tartsa mozdulatlanul. |
|
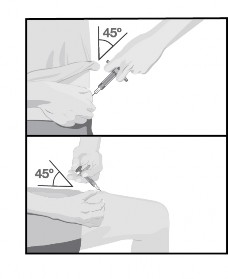
7. lépés |
Szúrja be a tűt a bőrébe körülbelül 45 fokos szögben, egy gyors, rövid mozdulattal.
Lassan nyomja be a dugattyút, egészen addig, amíg a folyadékot befecskendezte és az előretöltött fecskendő kiürült. |
-
Ne használja az előretöltött fecskendőt, ha az leesett vagy eltörött
-
Ne érintse meg a kezével a tűt, illetve ne hagyja, hogy a tű bármihez hozzáérjen.
-
Tartsa egyik kezében, szemmagasságban az előretöltött fecskendőt, hogy lássa a levegőt az előretöltött fecskendőben.
-
Normális, ha lát néhány csepp folyadékot kijönni a tűből

-
lépés
Amikor a beadás befejeződött, lassan húzza ki a bőrből a tűt, az előretöltött fecskendőt ugyanolyan szögben tartva.
Az injekció beadása után helyezzen egy vattapamacsot vagy gézdarabot a beadás helyére.
-
lépés
Az előretöltött fecskendőt dobja egy speciális gyűjtőedénybe a kezelőorvosa, a nővér vagy a gyógyszerésze útmutatásának megfelelően. Soha ne rakja vissza a tokot a tűre.
A tűvédő tokot, az alkoholos törlőt, a vattapamacsot vagy gézdarabot, a buborékcsomagolást és a csomagolást ki lehet dobni a háztartási hulladékba.







