B. BETEGTÁJÉKOZTATÓ
BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
Zarzio 30 millió E/0,5 ml oldatos injekció vagy infúzió előretöltött fecskendőben Zarzio 48 millió E/0,5 ml oldatos injekció vagy infúzió előretöltött fecskendőben
Filgrasztim
Mielőtt elkezdené alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót.
- - Tartsa meg a betegtájékoztatót, mert a benne szereplő információkra a későbbiekben is szüksége lehet.
- - További kérdéseivel forduljon orvosához vagy gyógyszerészéhez.
- - Ezt a gyógyszert az orvos Önnek írta fel. Ne adja át a készítményt másnak, mert számára ártalmas lehet még abban az esetben is, ha tünetei az Önéhez hasonlóak.
- - Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
A betegtájékoztató tartalma:
- 1. Milyen típusú gyógyszer a Zarzio és milyen betegségek esetén alkalmazható?
- 2. Tudnivalók a Zarzio alkalmazása előtt
- 3. Hogyan kell alkalmazni a Zarzio-t?
- 4. Lehetséges mellékhatások
- 5. Hogyan kell a Zarzio-t tárolni?
- 6. További információk
1. MILYEN TÍPUSÚ GYÓGYSZER A ZARZIO ÉS MILYEN BETEGSÉGEK ESETÉN ALKALMAZHATÓ?
A Zarzio hatóanyaga a filgrasztim. A filgrasztim a citokineknek nevezett fehérjecsoporthoz tartozik, és nagyon hasonlít az emberi szervezetben termelődő egyik természetes fehérjéhez (amelynek neve granulocita-kolónia stimuláló faktor [G-CSF]). A filgrasztim arra serkenti a csontvelőt (azt a szövetet, ahol az új vérsejtek termelődnek), hogy több fehérvérsejtet állítson elő, melyek segítenek a fertőzések leküzdésében. Ha a fehérvérsejtek száma túl alacsony (neutropénia), megnő a fertőzések veszélye.
Rákellenes kemoterápia
A Zarzio-t a neutropénia (alacsony fehérvérsejtszám) időtartamának és a lázas neutropénia (lázzal társult alacsony fehérvérsejtszám) előfordulásának csökkentésére használják gyermekek és felnőttek esetén. Ezeket a tüneteket a citotoxikus kemoterápiás kezelés (a gyorsan növekvő sejteket megsemmisítő gyógyszerek alkalmazása) okozhatja. A gyógyszer nem alkalmazható krónikus mieloid leukémiában (CML) és mielodiszpláziás szindrómában (MDS) szenvedő betegek esetén.
Csontvelő-átültetés
A Zarzio-t a neutropénia (alacsony fehérvérsejtszám) időtartamának csökkentésére használják csontvelő-átültetés után végzett magas dózisú kemoterápiát és az egész testen végzett sugárkezelést (radioterápia) követően olyan gyermekek és felnőttek esetén, akiknél fokozott a tartós, súlyos neutropénia kockázata.
A perifériás vér őssejtjeinek mobilizálása
A Zarzio-t a csontvelő stimulálására használják, hogy az perifériás vér progenitor sejteket (PBPC, egyfajta őssejt) szabadítson fel (mobilizáljon) a vérbe, melyek ott esetlegesen szaporodni kezdenek, és különböző fajta vérsejtekké alakulnak át: fehérvérsejtekké, vörösvértestekké és vérlemezkékké.
Ha Ön rákos beteg, a PBPC-ket eltávolítják a véréből, majd visszajuttatják azokat a kemoterápia és/vagy radioterápia után. Mivel a kemoterápia és/vagy radioterápia leállíthatja csontveleje működését, ez fel fogja gyorsítani a csontvelő regenerálódását.
Ha Ön más személynek ad őssejteket, a PBPC-ket eltávolítják a véréből, majd a kemoterápia és/vagy radioterápia után bejuttatják ezeket a fogadó személy vérébe.
Súlyos krónikus neutropénia
A Zarzio-t gyermekek és felnőttek esetén alkalmazzák a fehérvérsejtek számának növelésére, és azon fertőzések fellépésének és időtartamának csökkentésére, melyek a súlyos krónikus neutropénia specifikus formáival kapcsolatosak. Ezek a következők lehetnek: kongenitális (veleszületett), ciklikus (visszatérő), és idiopatikus (ismeretlen okból fellépő) neutropénia.
HIV (emberi immunhiány vírus) okozta fertőzéses neutropénia
A Zarzio-telőrehaladott HIV (emberi immunhiány vírus) okozta fertőzésben szenvedő betegek tartós neutropéniájának kezelésére használják a bakteriális fertőzések csökkentésére, amennyiben erre más kezelés nem alkalmazható.
2. TUDNIVALÓK A ZARZIO ALKALMAZÁSA ELŐTT
Ne alkalmazza a Zarzio-t
- - ha allergiás (túlérzékeny) a filgrasztimra vagy a Zarzio egyéb összetevőjére (ezek felsorolását a 6. „Mit tartalmaz a Zarzio“ c. fejezetben találja).
A Zarzio fokozott elővigyázatossággal alkalmazható
Kérjük, közölje kezelőorvosával
- - ha csontritkulásban (oszteoporózisban) szenved
- - ha sarlósejtes vérszegénységben szenved (a vörösvértestek megbetegedése, mely során a vörösvértestek sarló alakúvá válnak).
- - ha bizonyos vérrendellenességekben szenved, pl. mielodiszpláziás szindrómában (MDS) vagy krónikus mieloid leukémiában (CML).
- - ha Ön másik személynek ad őssejteket (donor) és antikoagulánsokkal (véralvadást segítő gyógyszerekkel) kezelik, vagy ha vérzési problémái vannak.
A kezelés ideje alatt alkalmazott egyéb gyógyszerek
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket is.
Terhesség és szoptatás
Feltétlenül közölje orvosával, ha terhes, azt gondolja, hogy terhes vagy tervezi a terhességet, mivel az orvos úgy dönthet, hogy Ön nem alkalmazhatja ezt a gyógyszer. A filgrasztim hatással lehet a teherbeesésre, ill. a terhesség fennmaradására.
Mivel nem ismeretes, hogy a filgrasztim bejut-e az anyatejbe, orvosa adott esetben úgy dönthet, hogy Ön nem használhatja ezt a gyógyszert szoptatás alatt.
Mielőtt bármilyen gyógyszert elkezdene szedni, beszélje meg kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A Zarzio nem befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
Fontos információk a Zarzio egyes összetevőiről
Ez a gyógyszer szorbitot (cukorfajta) tartalmaz. Amennyiben kezelőorvosa korábban már figyelmeztette Önt, hogy bizonyos cukrokra érzékeny (intoleráns), keresse fel orvosát, mielőtt elkezdi szedni ezt a gyógyszert.
3. HOGYAN KELL ALKALMAZNI A ZARZIO-T?
Az Ön számára szükséges Zarzio adag egyrészt attól az állapottól függ, amelyet a gyógyszerrel kezelnek, másrészt az Ön testtömegétől.
Rákellenes kemoterápia
A szokásos adag naponta 0,5 millió egység (E) testtömeg-kilogrammonként. Például, ha az Ön testsúlya 60 kg, az Ön napi adagja 30 millió egység (E) lesz. Az első dózis nem adható a citotoxikus kemoterápia utáni 24 órán belül. A kezelés időtartama maximum 14 nap. Bizonyos betegségekben azonban hosszabb, akár egy hónapig tartó kezelés is szükséges lehet.
Csontvelő-átültetés
A szokásos kezdő adag naponta 1 millió egység (E) testtömeg-kilogrammonként. Például, ha az Ön testsúlya 60 kg, az Ön napi adagja 60 millió egység (E) lesz. Az első adagot rendszerint legalább 24 órával a kemoterápia után, de az elvégzett csontvelő transzfúziót követő 24 órán belül fogja megkapni. Kezelőorvosa ezt követően vérvizsgálatot végez, hogy megállapítsa a kezelés hatásosságát, és azt is, hogy annak meddig kell tartania.
A perifériás vér őssejtek mobilizálása
- - Ha Ön saját maga számára ad őssejteket, a szokásos adag naponta 1 millió egység (E) testtömeg-kilogrammonként. A Zarzio-t 5-7 egymást követő napon át fogják Önnek adni. A Zarzio-kezelést az utolsó őssejt-begyűjtés befejezéséig fenn kell tartani.
- - Ha Ön kemoterápia után ad saját maga számára őssejteket, a szokásos adag naponta 0,5 millió egység (E) testtömeg-kilogrammonként. A Zarzio-t addig kell adni, amíg a várt legalacsonyabb fehérvérsejtszám elérése után a fehérvérsejtszám újra normalizálódik.
- - Ha Ön másik személynek ad őssejteket (donor), a szokásos adag naponta 1 millió egység (E) testtömeg-kilogrammonként. A Zarzio-kezelés 4-5 egymást követő napon át tart.
Kezelőorvosa rendszeresen elvégzett vérvizsgálatok segítségével dönti el, hogy melyik a legalkalmasabb időpont az őssejtek begyűjtésére.
Súlyos krónikus neutropénia
A szokásos kezdő adag testtömeg-kilogrammonként napi 0,5 millió és 1,2 millió egység (E) között mozog, amit egyetlen, vagy két adagban kap meg. Kezelőorvosa ezt követően vérvizsgálatot végez, hogy megállapítsa a kezelés hatásosságát, és azt is, hogy mekkora az Önnek megfelelő adag. Neutropénia esetén hosszú távú Zarzio-kezelésre is szükség lehet.
HIV (emberi immunhiány vírus) okozta fertőzéses neutropénia
A szokásos kezdő adag napi 0,1 millió és 0,4 millió egység (E) között mozog testtömeg-kilogrammonként. Orvosa rendszeres vérvizsgálatokkal ellenőrzi a kezelés hatásosságát. Amint a fehérvérsejtek száma visszatért a normális szintre, a kezelés gyakoriságát kevesebb mint napi egyszeri adagra lehet csökkenteni. A kezelőorvos továbbra is rendszeres vérvizsgálatokkal ellenőrzi az eredményeket, és a legmegfelelőbb adagot írja elő Önnek. A vér normális fehérvérsejtszámának fenntartása érdekében hosszú távú Zarzio kezelésre is szükség lehet.
Gyermekek és serdülők
Az ajánlott adag ugyanaz, mint a kemoterápiában részesülő felnőttek esetén.
Hogyan kell a Zarzio-t alkalmazni?
A Zarzio-t mindig az orvos által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát, a nővért vagy gyógyszerészét. Ezt a gyógyszert bőr alá adott injekció vagy vénába adott infúzió formájában adják be.
Orvosa dönthet úgy, hogy az Ön számára kényelmesebb, ha Ön adja be magának a Zarzio injekciót. Orvosa vagy a nővér megmutatja Önnek, hogyan kell beadnia magának az injekciót. Ne próbálkozzon az injekció beadásával, amíg nincs ebben gyakorlata!
A Zarzio injekció saját magának való beadásáról a betegtájékoztató végén talál utasításokat.
Ha az előírtnál több Zarzio-t alkalmazott
Ha az előírtnál több Zarzio-t alkalmazott, haladéktalanul keresse fel a nővért, orvosát vagy gyógyszerészét.
Ha elfelejtette alkalmazni a Zarzio-t
Ha elfelejtette alkalmazni a Zarzio-t, keresse fel orvosát és beszélje meg vele, hogy mikor adja be magának a következő adagot.
Ha idő előtt abbahagyja a Zarzio alkalmazását
Kezelőorvosa fogja közölni Önnel, hogy mikor hagyhatja abba a Zarzio alkalmazását. Az egészen szokványos, ha több Zarzio kezelési ciklusra van szükség.
4. LEHETSÉGES MELLÉKHATÁSOK
Mint minden gyógyszer, így a Zarzio is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Azonnal értesítse kezelőorvosát
- • köhög, lázas vagy nehézlégzés lép fel Önnél, mert ritkán előfordulhat, hogy tüdejében súlyos mellékhatások lépnek fel, pl. pneumónia (tüdőgyulladás), és respiratorikus distress (súlyos légzési elégtelenség)
- • ha fájdalmat érez a has bal felső területén vagy a bal vállcsúcsban, ugyanis ezek a lépet érintő probléma tünetei lehetnek
- • ha hirtelen légzési problémák lépnek fel, vagy szédül, ha megdagad az arca vagy a torka, illetve ha véraláfutást vagy kiütést észlel bőrén. Mivel ezek a tünetek súlyos allergiás reakcióra utalhatnak, hagyja abba az injekció adását és haladéktalanul forduljon orvoshoz.
A mellékhatások bizonyos gyakorisággal lépnek fel, melyek definíciója az alábbiakban található:
- • nagyon gyakori: 10-ből több mint egy betegnél fordul elő
- • gyakori: 100-ból 1-10 betegnél fordul elő
- • nem gyakori: 1000-ből 1-10 betegnél fordul elő
- • ritka: 10 000-ből 1-10 betegnél fordul elő
- • nagyon ritka: 10 000-ből kevesebb mint egy betegnél fordul elő
- • nem ismert: a rendelkezésre álló adatokból nem állapítható meg.
Nagyon gyakori mellékhatások:
- • csont-, ízületi és izomfájdalom
- • a húgysav és egyes enzimek szintjének emelkedése a vérben
- • a vércukorszint csökkenése
- • leukocitózis (a vérben található fehérvérsejtek számának kóros növekedése)
- • a vérlemezkék számának csökkenése (ami fokozza a vérzések és véraláfutások kockázatát)
- • a vörösvértestek számának csökkenése (ami sápadtságot, gyengeséget és légszomjat okozhat)
- • fejfájás
- • orrvérzés
- • lépmegnagyobbodás.
Gyakori mellékhatások
- • hasmenés
- • fájdalom az injekció beadási helyén
- • hajvesztés
- • bőrkiütés
- • májmegnagyobbodás
- • a bőr ereinek gyulladása
- • kálciumhiány a csontokban (osteoporosis)
- • léprendellenességek
Nem gyakori mellékhatások
- • vérnyomásesés
- • allergiás típusú reakciók, az anafilaxiát is ideértve (szédülés, súlyos vérnyomásesés, légzési nehézségek), angioödéma (az arc vagy a torok fájdalmas felduzzadása), légzési nehézségek, alacsony vérnyomás, bőrkiütés, csalánkiütés; ezek a reakciók felléphetnek a kezelés kezdetekor vagy annak során is
- • a reumás ízületi gyulladás (rheumatoid arthritis) és az ízületi gyulladás (arthritis) tüneteinek súlyosbodása
- • vér és fehérjék megjelenése a vizeletben
Ritka mellékhatások
- • érrendszeri betegségek, pl. veno-occlusiv betegség (a májat érintő betegség), vizenyő (ami a végtagok megdagadását okozhatja)
Nagyon ritka mellékhatások
- • vizelési nehézségek
- • Sweet-szindróma (lázzal járó, szilvakék, fájdalmas bőrkidudorodások megjelenése a végtagokon, néha az arcon és a nyakon)
- • tüdővizenyő, tüdővérzés, köhögéskor véres köpet, oxigénhiány, tüdőgyulladás (ami nehézlégzést, köhögést és lázat okozhat), és néhány esetben légzési elégtelenséghez vagy respiratorikus distressz szindrómához (ARDS, fokozott szapora légzés, nagyon rossz állapotban lévő betegekben) vezethet, ami halálos is lehet
- • sarlósejtes krízis (a vörösvértestek működésének akut kiesése) sarlósejtes vérszegénységben szenvedő betegek esetén.
- • lépszakadás, léprepedés
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
5. HOGYAN KELL A ZARZIO-T TÁROLNI?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és a fecskendő címkéjén feltüntetett lejárati idő (a dobozon Felhasználható:, ill. az injekció címkéjén EXP) után ne alkalmazza a Zarzio-t. A lejárati idő a megadott hónap utolsó napjára vonatkozik.
Hűtőszekrényben (2°C-8°C) tárolandó.
Az előretöltött fecskendő a fénytől való védelem érdekében a külső csomagolásban tárolandó.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy szükségtelenné vált gyógyszereit miként semmisítse meg. Ezek az intézkedések elősegítik a környezet védelmét.
6. TOVÁBBI INFORMÁCIÓK
Mit tartalmaz a Zarzio
- - A készítmény hatóanyaga a filgrasztim.
Zarzio 30 millió E/0,5 ml oldatos injekció vagy infúzió előretöltött fecskendőben: Minden 0,5 ml-es előretöltött fecskendő 30 millió egység (E) filgrasztimot tartalmaz, ami 60 millió E/ml-nek felel meg.
Zarzio 48 millió E/0,5 ml oldatos injekció vagy infúzió előretöltött fecskendőben: Minden 0,5 ml-es előretöltött fecskendő 48 millió egység (E) filgrasztimot tartalmaz, ami 96 millió E/ml-nek felel meg.
- - Egyéb összetevők: glutaminsav, szorbit (E 420), poliszorbát 80 és injekcióhoz való víz.
Milyen a Zarzio külleme és mit tartalmaz a csomagolás
A Zarzio tiszta, színtelen, ill. enyhén sárgás oldatos injekció vagy infúzió előretöltött fecskendőben.
A Zarzio 1, 3, 5, vagy 10 előretöltött fecskendőt tartalmazó csomagban, injekciós tűvel együtt, biztonsági tűvédővel vagy anélkül kerül forgalomba.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A forgalomba hozatali engedély jogosultja és a gyártó
Sandoz GmbH
Biochemiestrasse 10
A-6250 Kundl
Ausztria
A készítményhez kapcsolódó további kérdéseivel forduljon a forgalomba hozatali engedély jogosultjának helyi képviseletéhez:
België/Belgique/Belgien Sandoz nv-sa Telecom Gardens Medialaan 40 B-1800 Vilvoorde Tél/Tel: +32 27229797
| Luxembourg/Luxemburg Sandoz GmbH Biochemiestr. 10 A-6250 Kundl Tel: +43 5338 2000 |
България Представителство Сандоз д.д. Младост 4, Бизнес Парк София, Сграда 8Б, ет.6 София 1715 Тел.: +359 2 970 347 47
| Magyarország Sandoz Hungaria Kft. Timar u. 20 H-1034 Budapest Tel.: +36 1 430 2890 |
Česká republika Sandoz s.r.o. Jeseniova 30 CZ 130 00 Praha 3 Tel: +420 221 421 611 office.cz@sandoz.com
| Malta Sandoz GmbH Biochemiestr. 10 A-6250 Kundl Tel: +43 5338 2000 |
Danmark Sandoz A/S C.F. Tietgens Boulevard 40 DK-5220 Odense SØ Tlf: +45 63 95 10 00
| Nederland Sandoz B.V. Veluwezoom 22 NL-1327 AH Almere Tel: +31 36 52 41 600
|
Deutschland Sandoz Pharmaceuticals GmbH Raiffeisenstraße 11 D-83607 Holzkirchen Tel: +49 8024 902 4000 info@sandoz.de
| Norge Sandoz AS Jernbaneveien 4 N-1400 Ski Tlf: +47 64913000
|
Eesti Sandoz d.d. Eesti filiaal Pärnu mnt 105 EE – 11312 Tallinn Tel: +372 6652 400
| Österreich Sandoz GmbH Biochemiestr. 10 A-6250 Kundl Tel: +43 5338 2000 |
Ελλάδα Sandoz GmbH Biochemiestr. 10 A-6250 Kundl Tel: +43 5338 2000 | Polska Lek Polska Sp. z o.o. ul. Domaniewska 50 C PL – 02 672 Warszawa Tel.: +48 22 549 15 00
|
España Sandoz Farmacéutica, SA Avda. Osa Mayor, 4 E-28023 Aravaca (Madrid) Tel. +34 91 548 84 04 sandoz.responde@sandoz.com
| Portugal Sandoz Farmacêutica Lda. Alameda da Beloura, Edifício 1 2o andar – Esc. 15 P-2710−693 Sintra Tel: +351 21 924 19 19 sandoz.pt@sandoz.com |
France Sandoz SAS 49, avenue Georges Pompidou F-92593 Levallois-Perret Cedex Tél: + 33 1 49 64 48 00
| România S.C. Sandoz S.R.L. Str. Livezeni, Nr. 7A Târgu Mureş, 540472 - RO Tel: +40 265 208 120
|
Ireland Rowex Ltd Bantry Co. Cork - IRL Tel: + 353 27 50077 reg@rowa-pharma.ie
| Slovenija Lek farmacevtska družba d.d. Verovškova 57 SI-1526 Ljubljana Tel: +386 1 580 21 11 |
Ísland Sandoz A/S C.F. Tietgens Boulevard 40 DK-5220 Odense SØ Tlf: +45 63 95 10 00
| Slovenská republika Sandoz Pharmaceuticals d.d. Ružinovská 42 SK-82103 Bratislava Tel: +421 2 48 200 600
|
Italia Sandoz S.p.A. Largo Umberto Boccioni, 1 I-21040 Origgio / VA Tel: +39 02 96541
| Suomi/Finland Sandoz Oy Ab Rajatorpantie 41 B/Råtorpsvägen 41 B FIN-01640 Vantaa/Vanda Puh/Tel: +358 9 85 20 20 30
|
Κύπρος Sandoz GmbH Biochemiestr. 10 A-6250 Kundl Tel: +43 5338 2000 | Sverige Sandoz AB Berga Allé 1 E SE-254 52 Helsingborg Tel: + 46 42 152065 info.helsingborg@sandoz.com
|
Latvija Sandoz d.d. Pārstāvniecība Latvijā Meža iela 4 Rīga, LV-1048 Tel: +371 7 892 006
| United Kingdom Sandoz Ltd 37 Woolmer Way Bordon GU35 9QE – UK Tel: +44 1420 478301 uk.drugsafety@sandoz.com
|
Lietuva Sandoz Pharmaceuticals d.d filialas Šeimyniškių g. 3A LT – 09312 Vilnius Tel: +370 5 2636 038
|
|
A betegtájékoztató engedélyezésének dátuma
A gyógyszerről részletes információ az Európai Gyógyszerügynökség (EMEA) internetes honlapján ( http://www.emea.europa.eu /) található.
-------------------------------------------------------------------------------------------------------------------------
Információk az öninjekciózásról
Ez a rész azzal kapcsolatos információkat tartalmaz, hogy miként adhatja be magának a Zarzio injekciót. Fontos, hogy ne próbálja beadni magának az injekciót addig, amíg az orvostól vagy nővértől nem kapta meg az ehhez szükséges speciális kiképzést. A Zarzio biztonsági tűvédővel vagy anélkül kerül forgalomba és az orvosa vagy a nővér meg fogják Önnek mutatni, hogy kell az injekciót használni. Ha nem biztos abban, hogyan kell beadnia saját magának a készítményt vagy bármilyen egyéb kérdése van, kérjen segítséget az orvostól vagy a nővértől.
Hogyan fecskendezzem be magamnak az injekciót?
Az injekciót közvetlenül a bőr alatti szövetbe kell beadni. A befecskendezésnek ezt a módját szubkután (bőr alá adott) injekciónak nevezik. Orvosa vagy a nővér megmondja Önnek, hogy milyen gyakorisággal injekciózza magát.
Szükséges eszközök
A szubkután (bőr alá adott) injekció beadásához szükséges eszközök:
- 1. egy új Zarzio előretöltött fecskendő biztonsági tűvédővel vagy anélkül,
- 2. alkoholos vagy más, bőrfertőtlenítésre alkalmas törlőkendők,
- 3. amennyiben a Zarzio előretöltött fecskendőt biztonsági tűvédő nélkül alkalmazza: szúrásálló hulladékgyűjtő (amelynek falán nem hatol át a tű) a használt fecskendők biztonságos megsemmisítése érdekében.
Mit kell tennem, mielőtt beadom magamnak a Zarzio szubkután (bőr alá adott) injekciót?
- 1. Vegye ki a becsomagolt Zarzio-t a hűtőszekrényből. A Zarzio stabilitására nincs káros hatással, ha véletlenül fagyáspont alatti hőmérsékletnek van kitéve.
- 2. Ne rázza fel az előretöltött fecskendőt tartalmazó csomagolást.
- 3. Ellenőrizze, hogy az orvos által felírt adagnak megfelelő hatáserősségű kiszerelést tartja-e kezében.
- 4. Ellenőrizze a dobozon és a fecskendő címkéjén feltüntetett lejárati időt (Felhasználható:/EXP). Ne használja fel a készítményt, ha már elmúlt a feltüntetett hónap utolsó napja.
- 5. Ellenőrizze a Zarzio küllemét. Az oldat tiszta kell legyen. Ha az oldat zavaros vagy részecskéket tartalmaz, tilos felhasználni.
- 6. Kevésbé kellemetlen érzést kelt az injekció, ha az előretöltött fecskendőt 30 percig állni hagyja, hogy az oldat szobahőmérsékletűre melegedjen, vagy a fecskendőt pár percig óvatosan felmelegíti a kezében. Egyéb módon tilos felmelegíteni a Zarzio-t (pl. ne tegye mikrohullámú sütőbe vagy forró vízbe)!
- 7. Ne távolítsa el a fecskendő műanyag védőkupakját, csak akkor, ha készen áll az injekció beadására!
- 8. Alaposan mosson kezet!
- 9. Keressen egy kényelmes, jól megvilágított helyet, és helyezze elérhető közelségbe a fecskendőt, az alkoholos törlőket, és – amennyiben szükséges – a szúrásálló hulladékgyűjtőt.
Hogyan készítsem elő az injekciót?
A Zarzio befecskendezése előtt a következőket kell tennie:
- 1. A tűről óvatosan, csavarás nélkül húzza le a műanyag védőkupakot. Ne érintse meg a tűt, és ne nyomja meg a fecskendő dugattyúját.
- 2. Tartsa a tűvel ellátott fecskendőt felfelé, és ellenőrizze, hogy vannak-e a fecskendőben légbuborékok. Ha légbuborékokat talál, nyomja felfelé a dugattyút, és távolítsa el az összes levegőt a fecskendőből (ügyeljen rá, hogy folyadék ne távozzon a fecskendőből).
- 3. A fecskendő hengerén beosztás található. A fecskendő dugattyúját addig a számig (milliliter) nyomja, ami megfelel a kezelőorvos által Önnek felírt Zarzio adagnak.
- 4. Még egyszer ellenőrizze, hogy a megfelelő Zarzio adag van-e a fecskendőben.
- 5. Az előretöltött fecskendő most használatra kész.
Hová kell beadnom az injekciót?
Az injekció beadásának legmegfelelőbb helyei öninjekciózás esetén:
- - a comb felső része; és
- - a has, kivéve a köldök körüli területet.
Váltogassa az injekció beadási helyét, mert az a beadási helyen fellépő fájdalommal jár, ha mindig ugyanarra a helyre adja. Ha valaki más adja be az injekciót, a felkarok hátsó felszíne is alkalmazható.
Hogyan kell beadnom magamnak az injekciót?
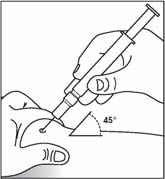
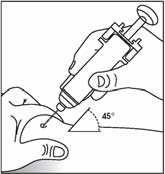
- 1. Fertőtlenítse a bőrfelületet az alkoholos kendővel, majd csípje a bőrt hüvelyk- és mutatóujja közé, anélkül, hogy erősen megszorítaná.
- 2. Nyomja bele kb. 45°-os szögben a bőrbe a tűt, ahogyan azt az orvos vagy a nővér mutatta.
- 3. Finoman húzza vissza a dugattyút, hogy ellenőrizze, a tű nem szúrt-e át valamilyen eret. Ha vért lát a fecskendőben, húzza ki a tűt, és szúrja be egy másik helyre.
Biztonsági tűvédő nélküli előretöltött fecskendő
- 4. Tartsa végig ujjaival összecsípve a bőrét, és a dugattyút lassan, egyenletesen nyomja befelé.
- 5. A folyadék befecskendezése után húzza ki a tűt, és engedje el az összecsípett bőrterületet.
- 6. Dobja be a fecskendőt a hulladékgyűjtőbe. Egy fecskendővel csakis egyszer adjon be injekciót!
Biztonsági tűvédő ellátott előretöltött fecskendő
- 4. Bőrét végig összecsípve tartva, nyomja meg a dugattyút lassan és egyenletesen egészen addig, amíg be nem adta a teljes adagot, és a dugattyú nem nyomható mélyebbre. Közben tartsa végig nyomva a dugattyút
- 5. A folyadék befecskendezése után húzza ki a tűt, a dugattyút továbbra is benyomva tartva, és engedje el az összecsípett bőrterületet.
- 6. Engedje el a dugattyút. A biztonsági tűvédő ekkor gyorsan elmozdul és elfedi a tű hegyét.
- 7. Egy fecskendővel csakis egyszer adjon be injekciót!
Ne feledje
Ha bármilyen problémája van, kérjen tanácsot az orvostól vagy a nővértől.
Hogyan kell kidobni a használt fecskendőket?
A használt fecskendők megsemmisítését a helyi előírások szerint kell végrehajtani.
Biztonsági tűvédő nélküli előretöltött fecskendő
- - A használt fecskendőre ne helyezze vissza a védőkupakot.
- - A használt fecskendőt dobja a szúrásálló hulladékgyűjtőbe és tartsa gyermekektől elzárva.
- - A teli hulladékgyűjtő tartályt az orvos a nővér, vagy a gyógyszerész utasításai alapján dobja el.
- - Használt fecskendőt SOHA ne dobjon ki normál háztartási hulladékgyűjtőbe!
Biztonsági tűvédő ellátott előretöltött fecskendő
- - A biztonsági tűvédő a tűszúrás okozta sérülések megelőzésére szolgál az injekció beadását követően, megsemmisítését illetően nincsenek speciális óvintézkedések. A fecskendőt az orvos a nővér vagy a gyógyszerész utasításai alapján dobja el.
-------------------------------------------------------------------------------------------------------------------------
Az alábbi információk kizárólag orvosoknak vagy más egészségügyi szakembereknek szólnak:
Felhasználás előtt az oldatot vizuális ellenőrzésnek kell alávetni. Csak a tiszta, részecskéktől mentes oldatot szabad felhasználni. A Zarzio stabilitására nincs káros hatással, ha véletlenül fagyáspont alatti hőmérsékletnek van kitéve.
A Zarzio nem tartalmaz tartósítószert: A lehetséges mikrobiális szennyeződések miatt a Zarzio fecskendők szigorúan egyszer használatos eszközök.
Alkalmazás előtti felhígítás (opcionális)
Szükség esetén a Zarzio 50 mg/ml (5%-os) glükóz-oldattal hígítható. A Zarzio nem hígítható nátrium-klorid oldattal.
A végső hígított koncentráció semmilyen körülmények között ne legyen 0,2 millió E/ml (2 mikrogramm/ml) értéknél alacsonyabb.
Azoknál a filgrasztimmal kezelt betegeknél, akiknek a készítményt < 1,5 millió E/ml (15 mikrogramm/ml) koncentrációban adják, humán szérum albumint (HSA) kell az oldathoz adni, hogy biztosítható legyen a végső, 2 mg/ml-es koncentráció.
Példa: 20 ml-es végső injekciós térfogat mellett a 30 millió E-nél (300 mikrogramm) kevesebb összdózisú filgrasztimhoz 0,2 ml 200 mg/ml (20%) koncentrációjú Ph.Eur minőségű humán albumin oldatot kell adni.
Ha a filgrasztimot 50 mg/ml (5%-os) glükóz-oldattal hígítják, az így elkészített oldat kompatibilis üveggel, különböző műanyagokkal, köztük PVC-vel, poliolefinnel (a polipropilén és polietilén egy kopolimerje) és polipropilénnel.
Hígítás után: A hígított oldatos infúzió használat közbeni kémiai és fizikai stabilitását 2-8°C-on bizonyítottan 24 órán keresztül őrzi meg. Mikrobiológiai szempontból a készítményt azonnal fel kell használni. Amennyiben nem kerül azonnali felhasználásra, a felbontás utáni tárolási idő és a felhasználás előtti tárolási körülmények a felhasználó felelősségét képezik, ami szokásos esetben, 2-8°C-on nem haladhatja meg a 24 órát, kivéve, ha a hígítást ellenőrzött, validált aszeptikus körülmények között végezték el.
Az előretöltött fecskendő alkalmazása biztonsági tűvédővel
A biztonsági tűvédő a tűszúrás okozta sérülések elkerülése érdekében az injekció beadása után elfedi a tűt. Ez nem befolyásolja a fecskendő használatát. Nyomja meg lassan és egyenletesen a dugattyút egészen addig, amíg be nem adta a teljes dózist, és a dugattyú nem nyomható mélyebbre. Húzza a betegből a fecskendőt, és közben tartsa fenn továbbra is a dugattyúra gyakorolt nyomást. A dugattyú elengedésekor a biztonsági tűvédő elfedi a tűt.
Az előretöltött fecskendő alkalmazása biztonsági tűvédő nélkül
A dózist a szokásos módon adja be.
Megsemmisítés
Bármilyen fel nem használt készítmény, illetve hulladékanyag megsemmisítését a helyi előírások szerint kell végrehajtani.