Betegtájékoztató: Információk a felhasználó számára
Caspofungin Onkogen 50 mg por oldatos infúzióhoz való koncentrátumhoz
Caspofungin Onkogen 70mg por oldatos infúzióhoz való koncentrátumhoz
kaszpofungin
Mielőtt Önnél vagy gyermekénél elkezdik alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára fontos információkat tartalmaz.
·· Tartsa meg a betegtájékoztatót, mert a benne szereplő információkra a későbbiekben is szüksége
lehet.
·· További kérdéseivel forduljon kezelőorvosához vagy a gondozását végző egészségügyi szakemberhez.
·· Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. Lásd 4. pont.
A betegtájékoztató tartalma
1. Milyen típusú gyógyszer a Caspofungin Onkogen és milyen betegségek esetén alkalmazható?
2. Tudnivalók a Caspofungin Onkogen alkalmazása előtt
3. Hogyan kell alkalmazni a Caspofungin Onkogen-t?
4. Lehetséges mellékhatások
5. Hogyan kell a Caspofungin Onkogen-t tárolni?
6. A csomagolás tartalma és egyéb információk
1. Milyen típusú gyógyszer a Caspofungin Onkogen és milyen betegségek esetén alkalmazható?
Milyen típusú gyógyszer a Caspofungin Onkogen
A Caspofungin Onkogen kaszpofungin nevű gyógyszert tartalmaz. Ez a gombaellenes gyógyszerek csoportjába tartozik.
Milyen betegségek esetén alkalmazható a Caspofungin Onkogen
A Caspofungin Onkogen az alábbi fertőzések kezelésére alkalmazható gyermekeknél, serdülőknél és felnőtteknél:
··
a beteg szöveteinek vagy szerveinek súlyos gombás
fertőzése (melyet „invazív kandidiázis”-nak neveznek).
Ezt a fertőzést a Candida nevű
(élesztő)gomba sejtjei okozzák.
Azok között, akik megkaphatják ezt a fajta
fertőzést, lehetnek olyan emberek, akik nemrégiben
műtéten estek át vagy gyenge az immunrendszerük. Az
ilyen típusú fertőzés leggyakoribb jelei az
antibiotikumokra nem reagáló láz és
hidegrázás.
·· a beteg orrában, arcüregeiben vagy tüdejében fellépő gombás fertőzések (melyeket „invazív aspergillózis”-nak neveznek), ha egyéb gombaellenes kezelések hatástalanok voltak vagy mellékhatásokat okoztak. Ezt a fertőzést az Aspergillus-nak nevezett penészgomba okozza. Azok között, akik megkaphatják ezt a fajta fertőzést, lehetnek olyan emberek, akik kemoterápiás kezelésben részesülnek, szervtranszplantáción estek át és akiknek gyenge az immunrendszerük.
·· gyanítható a gombás fertőzés, amennyiben a beteg lázas és alacsony a fehérvérsejtszáma, és az állapota antibiotikum-kezelés hatására nem javul. A gombás fertőzés kockázatának kitett emberek azok, akik nemrégiben műtéten estek át vagy gyenge az immunrendszerük.
Hogyan fejti ki hatását a Caspofungin Onkogen?
A Caspofungin Onkogen meggyengíti a gombasejteket, és megakadályozza, hogy a gomba megfelelően növekedjen. Ez megakadályozza a fertőzés terjedését, és elősegíti, hogy a szervezet természetes védekezőképessége által teljesen leküzdje a fertőzést.
2. Tudnivalók Caspofungin Onkogen alkalmazása előtt
Nem alkalmazható a Caspofungin Onkogen
· ha allergiás a kaszpofunginra, vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Ha nem biztos benne, beszéljen kezelőorvosával vagy a gondozását végző egészségügyi szakemberrel, mielőtt megkapja ezt a gyógyszert.
Figyelmeztetések és óvintézkedések
A Caspofungin Onkogen alkalmazása előtt beszéljen kezelőorvosával vagy a gondozását végző egészségügyi szakemberrel, ha:
·· allergiás bármilyen egyéb gyógyszerre.
·· májbetegségben szenved vagy korábban bármikor májbetegsége volt – a gyógyszer adagjának módosítására lehet szüksége.
·· ha jelenleg ciklosporint szed (az átültetett szerv kilökődésének megakadályozására vagy az
immunrendszer gyengítésére alkalmazzák) – mivel lehetséges, hogy kezelőorvosának kiegészítő vérvizsgálatokat kell kérnie az Ön kezelésének ideje alatt.
·· bármilyen egyéb egészségügyi problémája van vagy volt korábban.
Ha a fentiek közül bármelyik vonatkozik Önre (vagy Ön nem biztos benne), a Caspofungin Onkogen alkalmazása előtt beszéljen kezelőorvosával vagy a gondozását végző egészségügyi szakemberrel.
A Caspofungin Onkogen súlyos, a bőrrel kapcsolatos mellékhatásokat is okozhat, mint pl. a Stevens–Johnson szindróma (SJS) és a toxikus epidermális nekrolízis (TEN).
Egyéb gyógyszerek és Caspofungin Onkogen
Feltétlenül tájékoztassa kezelőorvosát vagy a gondozását végző egészségügyi szakembert a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről. Ez vonatkozik a vény nélkül kapható készítményekre, ide értve a gyógynövény-készítményeket is. Erre azért van szükség, mert a Caspofungin Onkogen befolyásolhatja néhány egyéb gyógyszer hatását és néhány egyéb gyógyszer befolyásolhatja a Caspofungin Onkogen hatását.
Tájékoztassa kezelőorvosát vagy a gondozását végző egészségügyi szakembert, ha Ön az alábbi gyógyszerek bármelyikét szedi:
·· ciklosporin vagy takrolimusz (az átültetett szerv kilökődésének megakadályozására vagy az immunrendszer gyengítésére alkalmazzák), mivel lehetséges, hogy kezelőorvosának kiegészítő vérvizsgálatokat kell kérnie az Ön kezelésének ideje alatt
·· egyes HIV-gyógyszerek, például efavirenz vagy nevirapin
·· fenitoin vagy karbamazepin (epilepszia kezelésére használatosak)
·· dexametazon (egy szteroid)
·· rifampicin (egy antibiotikum).
Ha a fentiek közül bármelyik vonatkozik Önre (vagy Ön nem biztos benne), a Caspofungin Onkogen beadása előtt beszéljen kezelőorvosával vagy a gondozását végző egészségügyi szakemberrel.
Terhesség és szoptatás
Ha Ön terhes vagy szoptat, illetve, ha fennáll Önnél a terhesség lehetősége, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával.
A Caspofungin Onkogen terhes nőknél történő alkalmazását nem vizsgálták. Terhesség esetén a készítmény csak akkor alkalmazható, ha a várható előny nagyobb, mint a magzatot érintő lehetséges kockázat.
Caspofungin Onkogen–kezelésben részesülő nők nem szoptathatnak.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Nem áll rendelkezésre olyan információ, mely alapján feltételezhető lenne, hogy a Caspofungin Onkogen befolyásolná a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
A Caspofungin Onkogen szacharózt tartalmaz
A Caspofungin Onkogen szacharózt (egy cukorfajtát) tartalmaz. Amennyiben kezelőorvosa korábban már figyelmeztette Önt, hogy az Ön szervezete bizonyos cukrokat nem tolerál vagy nem tud megemészteni, beszéljen kezelőorvosával, a gondozását végző egészségügyi szakemberrel vagy gyógyszerészével a gyógyszer alkalmazásának megkezdése előtt.
3. Hogyan kell alkalmazni a Caspofungin Onkogent?
A Caspofungin Onkogent-t mindig egy egészségügyi szakember készíti el, és adja be Önnek. A Caspofungin Onkogent-t Ön:
·· naponta egyszer fogja megkapni
·· lassan befecskendezve a vénájába (intravénás infúzió formájában)
·· körülbelül 1 óra alatt beadva.
Kezelőorvosa határozza meg a kezelés időtartamát, illetve a napi Caspofungin Onkogen adagot. Kezelőorvosa figyelemmel fogja kísérni, hogyan fejti ki a gyógyszer hatását az Ön szervezetében.
80 kg testsúly felett szükséges lehet az adag módosítása.
Alkalmazása gyermekeknél és serdülőknél
A gyermekeknél és serdülőknél alkalmazott adagok eltérhetnek a felnőtt adagoktól.
Ha az előírtnál több Caspofungin Onkogent-t kapott
Kezelőorvosa fogja eldönteni, hogy Önnek naponta milyen mennyiségben és milyen hosszú ideig kell a Caspofungin Onkogen-t megkapnia. Amennyiben Önt nyugtalanítja, hogy esetleg túl nagy Caspofungin Onkogen adagot kapott, forduljon haladéktalanul kezelőorvosához vagy a gondozását végző egészségügyi szakemberhez.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a készítmény is okozhat mellékhatásokat, melyek azonban nem mindenkinél jelentkeznek.
Azonnal jelezze kezelőorvosának vagy a gondozását végző egészségügyi szakembernek, ha az alábbi mellékhatások bármelyikét tapasztalja – Önnek sürgős orvosi beavatkozásra lehet szüksége:
· bőrkiütések, viszketés, melegség érzete, az arc, ajkak vagy torok duzzanata, illetve nehézlégzés – Önnek a gyógyszerrel szemben úgynevezett hisztamin-reakciója alakulhatott ki.
· zihálással vagy bőrkiütésekkel együtt fellépő nehézlégzés, amely súlyosbodik – Önnek allergiás reakciója lehet a gyógyszerre.
· köhögés, súlyos légzési nehézségek – ha Ön felnőtt és invazív aspergillózisban szenved, súlyos légzési probléma léphetett fel Önnél, mely a légzés összeomlását eredményezheti.
· bőrkiütés, bőrhámlás, nyálkahártyafekélyek, csalánkiütés, nagy területen hámló bőr.
Mint minden más vényköteles gyógyszer esetében, néhány mellékhatás súlyos lehet. További információért forduljon kezelőorvosához.
A felnőttek esetében tapasztalt további mellékhatások:
Gyakori: 10 közül legfeljebb 1 embert érinthet:
· Csökkent hemoglobinszint (az oxigénszállító anyag csökkenése a vérben), csökkent fehérvérsejt-szám
· Csökkent albuminszint (egy fehérjefajta) a vérben, csökkent vagy alacsony káliumszint a vérben
· Fejfájás
· Vénagyulladás
· Légzési nehézség
· Hasmenés, hányinger vagy hányás
· Néhány laboratóriumi vérvizsgálat eredményének megváltozása (többek között egyes
májfunkciós értékek megemelkedése)
· Viszketés, bőrkiütések, bőrpír vagy a szokásosnál erősebb verejtékezés
· Ízületi fájdalom
· Hidegrázás, láz
· Viszketés az injekció beadásának a helyén.
Nem gyakori: 100 közül legfeljebb 1 embert érinthet:
· Néhány laboratóriumi vérvizsgálat eredményének megváltozása (beleértve a véralvadással,
vérlemezkékkel, vörösvértestekkel és fehérvérsejtekkel kapcsolatos megbetegedéseket is)
· Étvágycsökkenés, a testfolyadék mennyiségének növekedése, a szervezet sóháztartásának
egyensúlyzavara, magas vércukorszint, alacsony kalciumszint a vérben, alacsony
magnéziumszint a vérben, a vér savmennyiségének növekedése
Zavartság, idegesség, alvásképtelenség
Szédülés, érzés- vagy érzékelés-csökkenés vagy érzékenység (különösen a bőrön), remegés, álmosság, az ízérzékelés megváltozása, bizsergés vagy zsibbadás
· Homályos látás, fokozott könnyezés, szemhéjduzzanat, a szemfehérje besárgulása
· Gyors vagy szabálytalan szívverés érzése, felgyorsult szívverés, szabálytalan szívverés,
szívritmuszavar, szívelégtelenség
· Kipirulás, hőhullám, magas vérnyomás, alacsony vérnyomás, vörösség a véna mentén, mely
érintésre rendkívül érzékeny
· A légutakat körülvevő izomkötegek megfeszülése, mely sípoló légzést vagy köhögést vált ki,
felgyorsult légzésszám, légszomj, ami felébreszti Önt álmából, oxigénhiány a vérben, rendellenes légzési hangok, hóropogásszerű hangok a tüdőben, sípoló légzés, orrdugulás, köhögés, torokfájás
· Hasfájás, gyomortáji fájdalom, felfúvódás, székrekedés, nyelési nehézség, szájszárazság, gyomorrontás, bélgázürítés, kellemetlen érzés a gyomorban, duzzanat a belek körül felszaporodott folyadék miatt
· Csökkent epetermelés, májmegnagyobbodás, a bőr és/vagy a szemfehérje besárgulása, gyógyszer vagy kémiai szer okozta májkárosodás, májbetegség
· Kóros bőrszövet, tesztszerte fellépő viszketés, csalánkiütés, különböző formájú bőrkiütések, bőrrendellenesség, vörös, gyakran viszkető foltok a karokon és lábakon, valamint néha az arcon és a testfelület többi részén is
· Hátfájás, kar- vagy lábfájdalom, csontfájdalom, izomfájdalom, izomgyengeség
· A vesefunkció beszűkülése, a veseműködés hirtelen leállása
· Fájdalom a kanül helyén, az injekció beadásának helyén fellépő panaszok (vörösség, kemény csomó,
fájdalom, duzzanat, irritáció, bőrkiütés, csalánkiütés, folyadékszivárgás a katéterből a szövetekbe),
vénagyulladás az injekció beadásának a helyén
· Emelkedett vérnyomás és néhány laboratóriumi vérvizsgálat (beleértve az elektrolitszint a
vesében és véralvadás-vizsgálat is) eredményének megváltozása, az Ön által szedett,
immunrendszert gyengítő gyógyszerek szintjének emelkedése
· Kellemetlen érzés a mellkasban, mellkasi fájdalom, a testhőmérséklet változásának érzése,
általános rossz közérzet, általános fájdalom, az arc duzzanata, a bokák, a kezek vagy a lábak duzzanata, vizenyős duzzanat, érzékenység, fáradtságérzés.
Mellékhatások gyermekeknél és serdülőknél
Nagyon gyakori: 10 ember közül több, mint 1 embert érinthet:
Láz
Gyakori: 10 ember közül legfeljebb 1 embert érinthet
· Fejfájás
· Felgyorsult szívverés
· Kipirulás, alacsony vérnyomás
· Néhány laboratóriumi vérvizsgálat eredményének megváltozása (egyes májfunkciós értékek
megemelkedése)
· Viszketés, bőrkiütés
· Fájdalom a katéter helyén
· Hidegrázás
· Eltérés néhány laboratóriumi vérvizsgálat eredményében.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, a gondozását végző egészségügyi szakembert vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül.
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Caspofungin Onkogen-t tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és az injekciós üvegen feltüntetett lejárati idő után ne alkalmazza ezt a gyógyszert (az első két számjegy a hónapot, a következő négy számjegy az évet jelöli). A lejárati idő az adott hónap utolsó napjára vonatkozik.
Felbontatlan injekciós üvegek: Hűtőszekrényben (2°C - 8°C) tárolandó.
A Caspofingin Onkogen-t a feloldást követően azonnal fel kell használni. Erre azért van szükség, mert a készítmény nem tartalmaz olyan összetevőt, amely megakadályozná a baktériumok elszaporodását. Kizárólag képzett egészségügyi szakember készítheti el a gyógyszert, a teljes használati utasítás elolvasása után (lásd alább „Előírás a Caspofungin Onkogen feloldására és hígítására”).
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. Milyen a Caspofungin Onkogen külleme és mit tartalmaz a csomagolás?
Mit tartalmaz a Caspofungin Onkogen
Minden 50 mg-os Caspofungin Onkogen injekciós üveg 50 mg kaszpofungint tartalmaz. Minden 70 mg-os Caspofungin Onkogen injekciós üveg 70 mg kaszpofungint tartalmaz.
Milyen a Caspofungin Onkogen külleme és mit tartalmaz a csomagolás?
A Caspofungin Onkogen feloldás előtt steril, fehér vagy csaknem fehér színű, liofilizált por.
10 ml-es I-es típusú injekciós üveg, butil-dugóval, lepattintható alumínium kupakkal.
CASPOFUNGIN ONKOGEN 50 mg por oldatos infúzióhoz való koncentrátumhoz
10 ml-es átlátszó, I-es típusú injekciós üveg, szürke brómbutil gumidugóval és lepattintható piros PP védőlappal ellátott rollnizott alumínium kupakkal lezárva.
1 db port tartalmazó injekciós üveg dobozban.
CASPOFUNGIN ONKOGEN 70 mg por oldatos infúzióhoz való koncentrátumhoz
10 ml-es átlátszó, I-es típusú injekciós üveg, szürke brómbutil gumidugóval és lepattintható narancssárga PP védőlappal ellátott rollnizott alumínium kupakkal lezárva.
1 db port tartalmazó injekciós üveg dobozban.
A forgalomba hozatali engedély jogosultja
Onkogen Kft.
1037 Budapest, Jablonka út 29/B.
Gyártó
Pharmathen S.A.
Dervenakion str., Pallini, Attiki
15351, Görögország
Pharmadox Healthcare Ltd
KW20A Kordin Industrial Park, Paola
PLA 3000, Málta
CASPOFUNGIN ONKOGEN 50 mg por oldatos infúzióhoz való koncentrátumhoz
OGYI-T-23166/01 1x injekciós üvegben
CASPOFUNGIN ONKOGEN 70 mg por oldatos infúzióhoz való koncentrátumhoz
OGYI-T-23166/02 1x injekciós üvegben
A betegtájékoztató legutóbbi felülvizsgálatának dátuma: 2017. február
-----------------------------------------------------------------------------------------------------------------
Az alábbi információk kizárólag orvosoknak vagy egészségügyi szakembereknek szólnak:
Előírás a CASPOFUNGIN ONKOGEN feloldására és higítására:
A CASPOFUNGIN ONKOGEN feloldása
NE HASZNÁLJON GLÜKÓZT TARTALMAZÓ OLDÓSZERT, mivel a CASPOFUNGIN ONKOGEN glükózt tartalmazó oldószerben nem stabil. A CASPOFUNGIN ONKOGEN-T MÁS GYÓGYSZEREKKEL NE KEVERJE, ÉS INFÚZIÓBAN NE ADJA EGYÜTT, mivel nem állnak rendelkezésre adatok a CASPOFUNGIN ONKOGEN más intravénás anyagokkal, adalékanyagokkal vagy gyógyszerekkel való összeférhetőségéről. Az infúziós oldatot vizuálisan ellenőrizni kell, hogy nem tartalmaz-e lebegő részecskéket vagy elszíneződést.
Injekcióhoz való vízben történő feloldást követően az elkészített oldat kémiai és fizikai stabilitása 2°C‑8°C–on és 25°C-on 24 órán át igazolt.
Mikrobiológiai szempontból a készítményt azonnal fel kell használni, kivéve, ha a felbontás/elkészítés módszere kizárja a mikrobiológiai szennyeződés kockázatát.
Amennyiben nem használják fel azonnal, a felhasználásig az eltartási idő és a tárolási körülmények a felhasználó felelőssége.
A betegek számára tovább hígított infúziós oldat kémiai és fizikai stabilitása 2-8°C –on és 25°C-on 48 órán át igazolt, amennyiben a hígítás 9 mg/ml (0,9 %), 4,5 mg/ml (0,45 %), vagy 2,25 mg/ml (0,225 %) infúzióhoz való nátrium-klorid oldattal, vagy pedig Ringer-laktát oldattal történt.
Mikrobiológiai szempontból a készítményt azonnal fel kell használni. Amennyiben nem használják fel azonnal, a felhasználásig az eltartási idő és a tárolási körülmények a felhasználó a felelőssége, amely általános esetben nem haladhatja meg a 24 órát 2°C-8°C-on tárolva, kivéve, ha a feloldás és a hígítás ellenőrzött és validált aszeptikus körülmények között történt.
A CASPOFUNGIN ONKOGEN 50 mg és 70 mg por oldatos infúzióhoz való koncentrátumhoz készítmény tartósítószereket nem tartalmaz.
Bármilyen fel nem használt gyógyszer, illetve hulladékanyag megsemmisítését a gyógyszerekre vonatkozó előírások szerint kell végrehajtani.
HASZNÁLATI UTASÍTÁS FELNŐTT BETEGEK RÉSZÉRE
1. lépés: A hagyományos injekciós üveg tartalmának feloldása
Az 50 mg-os por feloldásához egy ideig az injekciós üveget szobahőmérsékleten kell tartani, és aszeptikus körülmények között hozzá kell adni 10,5 ml injekcióhoz való vizet. Az injekciós üvegekben elkészített oldat koncentrációja 5,2 mg/ml lesz.
A 70 mg-os por feloldásához egy ideig az injekciós üveget szobahőmérsékleten kell tartani, és aszeptikus körülmények között hozzá kell adni 10,5 ml injekcióhoz való vizet. Az injekciós üvegekben elkészített oldat koncentrációja 7,2 mg/ml lesz.
A fehér vagy csaknem fehér színű, liofilizált por teljes mértékben feloldódik. Kíméletesen kell keverni mindaddig, amíg tiszta oldatot nem kapunk. A feloldást követően nyert oldatot vizuálisan ellenőrizni kell, hogy nem tartalmaz-e részecskéket vagy elszíneződést. Injekcióhoz való vízben történő feloldást követően az elkészített oldat 2°C -8°C-on és 25°C-on legfeljebb 24 órán át tárolható.
2. lépés: Az elkészített CASPOFUNGIN ONKOGEN hozzáadása a betegeknek adandó infúziós oldathoz
A kész infúziós oldat készítéséhez használható oldószerek: nátrium-klorid oldatos injekció vagy Ringer-laktát oldat. Az infúziós oldatot úgy kell elkészíteni, hogy egy 250 ml-es infúziós zsák vagy üveg tartalmához aszeptikus körülmények között hozzá kell adni a feloldott koncentrátum megfelelő mennyiségét (ahogyan azt az alábbi táblázat mutatja). Ha ez orvosilag indokolt, a napi 50 mg-os vagy 35 mg-os napi adagok esetében csökkentett térfogatú (100 ml-es) infúziók is használhatóak.
Nem használható fel az oldat, ha az zavaros vagylátható részecskéket tartalmaz.
AZ INFÚZIÓS OLDAT ELKÉSZÍTÉSE FELNŐTTEK RÉSZÉRE
|
Dózis* |
Az intravénás zsákba vagy üvegbe átvitelre kerülő elkészített CASPOFUNGIN ONKOGEN térfogata
|
Standard készítmény (250 ml-hez hozzáadott, elkészített CASPOFUNGIN ONKOGEN) végső koncentrációja |
Csökkentett
térfogatú infúzió |
|
50 mg |
10 ml |
0,20 mg/ml |
- |
|
50 mg csökkent térfogatnál |
10 ml |
- |
0,47 mg/ml |
|
35 mg közepesen súlyos májkárosodás esetén (egy 50 mg-os injekciós üvegből) |
7 ml |
0,14 mg/ml |
- |
|
35 mg közepesen súlyos májkárosodás esetén (egy 50 mg-os injekciós üvegből) csökkentett térfogatnál |
7 ml |
- |
0,34 mg/ml |
|
70 mg |
10 ml |
0,28 mg/ml |
Nem javasolt |
|
70 mg (két 50-mg-os injekciós üvegből)** |
14 ml |
0,28 mg/ml |
Nem javasolt |
|
35 mg közepesen súlyos májkárosodás esetén (egy 70 mg-os injekciós üvegből) |
5 ml |
0,14 mg/ml |
0,34 mg/ml |
* Minden injekciós üveg tartalmának feloldásához 10,5 ml-t kell használni
*Amennyiben a 70 mg-os injekciós üveg nem elérhető, a 70 mg-os dózis elkészíthető két 50 mg-os injekciósüvegből is.
HASZNÁLATI UTASÍTÁS GYERMEKGYÓGYÁSZATI BETEGEK RÉSZÉRE
A testfelszín területének (Body Surface Area, BSA) kiszámítása gyermekgyógyászati adagoláshoz
Az infúzió elkészítése előtt a következő képlet segítségével (Mosteller-képlet) kell kiszámolni a beteg testfelszínének (BSA) területét:
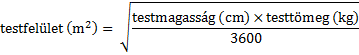
A 70 mg/m2 infúzió elkészítése 3 hónaposnál idősebb gyermekgyógyászati betegek részére (50 mg-os injekciós üveget használva)
1. Meg kell határozni a gyermekgyógyászati betegnél alkalmazandó tényleges telítő dózist a beteg (fentiek szerint kiszámolt) BSA-értéke és a következő egyenlet segítségével:
BSA (m2) x 70 mg/m2 = Telítő dózis
Függetlenül a beteg kiszámolt adagjától, az 1. napon a maximális telítő dózis nem haladhatja meg a 70 mg-ot.
2. A lehűtött CASPOFUNGIN ONKOGEN injekciós üveget szobahőmérsékletre kell helyezni.
3. Aszeptikus körülmények között hozzá kell adni 10,5 ml injekcióhoz való vizet.a Ez az elkészített oldat maximum 24 órán át tárolható legfeljebb 25°C-on.b Az injekciós üvegben így elkészített kaszpofungin végső koncentrációja 5,2 mg/ml lesz.
4. Fel kell szívni az (1. pont szerint) kiszámolt telítő dózisnak megfelelő mennyiségű gyógyszert az injekciós üvegből. Aszeptikus körülmények között hozzá kell adni a feloldott CASPOFUNGIN ONKOGEN ezen mennyiségét (ml)c egy 250 ml 0,9%-os, 0,45%-os, vagy 0,225%-os nátrium-klorid oldatot vagy Ringer-laktát oldatot tartalmazó IV-zsákhoz (vagy üveghez). Ha szükséges, a feloldott CASPOFUNGIN ONKOGEN mennyisége (ml)c 0,9%-os, 0,45%-os vagy 0,225%-os, csökkentett térfogatú nátrium-klorid oldathoz vagy Ringer-laktát oldathoz is hozzáadható úgy, hogy a 0,5 mg/ml végső koncentrációt ne lépjük túl. Ezt az infúziós oldatot 24 órán belül fel kell használni legfeljebb °C-on tárolva, vagy 48 órán belül fel kell használni, ha azt hűtve tárolják
2°C -8°C közötti hőmérsékleten.
Az 50 mg/m2 infúzió elkészítése 3 hónaposnál idősebb gyermekgyógyászati betegek részére (50 mg-os injekciós üveget használva)
1. Meg kell határozni a gyermekgyógyászati betegnél alkalmazandó tényleges telítő dózist a beteg (fentiek szerint kiszámolt) BSA-értéke és a következő egyenlet segítségével:
BSA (m2) x 70 mg/m2 = Telítő dózis
Függetlenül a beteg kiszámolt adagjától, az 1. napon a maximális telítő dózis nem haladhatja meg a 70 mg-ot.
2. A lehűtött CASPOFUNGIN ONKOGEN injekciós üveget szobahőmérsékletre kell helyezni.
3. Aszeptikus körülmények között hozzá kell adni 10,5 ml injekcióhoz való vizet.a Ez az elkészített oldat maximum 24 órán át tárolható legfeljebb 25°C-on.b Az injekciós üvegben így elkészített kaszpofungin végső koncentrációja 5,2 mg/ml lesz.
4. Fel kell szívni az (1. pont szerint) kiszámolt telítő dózisnak megfelelő mennyiségű gyógyszert az injekciós üvegből. Aszeptikus körülmények között hozzá kell adni a feloldott CASPOFUNGIN ONKOGEN ezen mennyiségét (ml)c egy 250 ml 0,9%-os, 0,45%-os, vagy 0,225%-os nátrium-klorid oldatot vagy Ringer-laktát oldatot tartalmazó IV-zsákhoz (vagy üveghez). Ha szükséges, a feloldott CASPOFUNGIN ONKOGEN mennyisége (ml)c 0,9%-os, 0,45%-os vagy 0,225%-os, csökkentett térfogatú nátrium-klorid oldathoz vagy Ringer-laktát oldathoz is hozzáadható úgy, hogy a 0,5 mg/ml végső koncentrációt ne lépjük túl. Ezt az infúziós oldatot 24 órán belül fel kell használni legfeljebb 25°C-on tárolva, vagy 48 órán belül fel kell használni, ha azt hűtve tárolják 2°C -8°C közötti hőmérsékleten.
A 70 mg/m2 infúzió elkészítése 3 hónaposnál idősebb gyermekgyógyászati betegek részére (70 mg-os injekciós üveget használva)
1. Meg kell határozni a gyermekgyógyászati betegnél alkalmazandó tényleges telítő dózist a beteg (fentiek szerint kiszámolt) BSA-értéke és a következő egyenlet segítségével:
BSA (m2) x 70 mg/m2 = Telítő dózis
Függetlenül a beteg kiszámolt adagjától, az 1. napon a maximális telítő dózis nem haladhatja meg a 70 mg-ot.
2. A lehűtött CASPOFUNGIN ONKOGEN injekciós üveget szobahőmérsékletre kell helyezni.
3. Aszeptikus körülmények között hozzá kell adni 10,5 ml injekcióhoz való vizet.a Ez az elkészített oldat maximum 24 óráig tárolható legfeljebb 25°C-on vagy annál alacsonyabb hőmérsékleten tárolható.b Az injekciós üvegben így elkészített kaszpofungin végső koncentrációja 7,2 mg/ml lesz.
4. Fel kell szívni az (1. pont szerint) kiszámolt telítő dózisnak megfelelő mennyiségű gyógyszert az injekciós üvegből. Aszeptikus körülmények között hozzá kell adni a feloldott CASPOFUNGIN ONKOGEN ezen mennyiségét (ml)d egy 250 ml 0,9%-os, 0,45%-os, vagy 0,225%-os nátrium-klorid oldatot vagy Ringer-laktát oldatot tartalmazó IV-zsákhoz (vagy üveghez). Ha szükséges, a feloldott CASPOFUNGIN ONKOGEN mennyisége (ml)d 0,9%-os, 0,45%-os vagy 0,225%-os, csökkentett térfogatú nátrium-klorid oldathoz vagy Ringer-laktát oldathoz is hozzáadható úgy, hogy a 0,5 mg/ml végső koncentrációt ne lépjük túl. Ezt az infúziós oldatot 24 órán belül fel kell használni legfeljebb 25°C-on tárolva, vagy 48 órán belül fel kell használni, ha azt hűtve tárolják 2°C-8°C közötti hőmérsékleten.
Az 50 mg/m2 infúzió elkészítése 3 hónaposnál idősebb gyermekgyógyászati betegek részére (50 mg-os injekciós üveget használva)
1. Meg kell határozni a gyermekgyógyászati betegnél alkalmazandó tényleges telítő dózist a beteg (fentiek szerint kiszámolt) BSA-értéke és a következő egyenlet segítségével:
BSA (m2) x 70 mg/m2 = Telítő dózis
Függetlenül a beteg kiszámolt adagjától, az 1. napon a maximális telítő dózis nem haladhatja meg a 70 mg-ot.
2. A lehűtött CASPOFUNGIN ONKOGEN injekciós üveget szobahőmérsékletre kell helyezni.
3. Aszeptikus körülmények között hozzá kell adni 10,5 ml injekcióhoz való vizet.a Ez az elkészített oldat maximum 24 óráig tárolható legfeljebb 25°C-on.b Az injekciós üvegben így elkészített kaszpofungin végső koncentrációja 7,2 mg/ml lesz.
4. Fel kell szívni az (1. pont szerint) kiszámolt telítő dózisnak megfelelő mennyiségű gyógyszert az injekciós üvegből. Aszeptikus körülmények között hozzá kell adni a feloldott CASPOFUNGIN ONKOGEN ezen mennyiségét (ml)d egy 250 ml 0,9%-os, 0,45%-os, vagy 0,225%-os nátrium-klorid oldatot vagy Ringer-laktát oldatot tartalmazó IV-zsákhoz (vagy üveghez). Ha szükséges, a feloldott CASPOFUNGIN ONKOGEN mennyisége (ml)d 0,9%-os, 0,45%-os vagy 0,225%-os, csökkentett térfogatú nátrium-klorid oldathoz vagy Ringer-laktát oldathoz is hozzáadható úgy, hogy a 0,5 mg/ml végső koncentrációt ne lépjük túl. Ezt az infúziós oldatot 24 órán belül fel kell használni legfeljeb 25°C-on tárolva, vagy 48 órán belül fel kell használni, ha azt hűtve tárolják 2°C -8°C közötti hőmérsékleten.
|
Az elkészítésre vonatkozó megjegyzések: a A fehér-vagy csaknem fehér színű, liofilizált por teljes mértékben feloldódik. Kíméletesen kell keverni mindaddig, amíg tiszta oldatot nem kapunk. b A feloldott oldatot vizuálisan ellenőrizni kell a feloldás során és az infúzió alkalmazását megelőzően, hogy nem tartalmaz-e részecskéket vagy elszíneződést. Nem használható fel az oldatot, ha az zavaros vagy látható részecskéket tartalmaz. c A CASPOFUNGIN ONKOGEN kiszerelése biztosítja, hogy 10 ml felszívásakor az oldat a címkén feltüntetett teljes adagot (50 mg) tartalmazza. d A CASPOFUNGIN ONKOGEN kiszerelése biztosítja, hogy 10 ml felszívásakor az oldat a címkén feltüntetett teljes adagot (70 mg) tartalmazza. |