Betegtájékoztató: Információk a felhasználó számára
Diphereline SR 3,75 mg por és oldószer retard
szuszpenziós injekcióhoz
triptorelin
Mielőtt elkezdi alkalmazni
ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az
Ön számára fontos információkat tartalmaz.
-
Tartsa meg a betegtájékoztatót,
mert a benne szereplő információkra a későbbiekben is szüksége lehet.
-
További kérdéseivel forduljon
kezelőorvosához, gyógyszerészéhez vagy a
gondozását végző egészségügyi szakemberhez.
-
Ezt a gyógyszert az orvos
kizárólag Önnek írta fel. Ne adja át a készítményt másnak, mert számára
ártalmas lehet még abban az esetben is, ha a betegsége tünetei az Önéhez
hasonlóak.
-
Ha Önnél bármilyen mellékhatás
jelentkezik, tájékoztassa erről kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Ez
a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is
vonatkozik. Lásd 4. pont
A
betegtájékoztató tartalma:
1. Milyen típusú gyógyszer a Diphereline SR 3,75
mg por és oldószer retard szuszpenziós injekcióhoz (továbbiakban Diphereline SR
3,75 mg injekció) és milyen betegségek esetén alkalmazható?
2. Tudnivalók a Diphereline SR 3,75 mg injekció
alkalmazása előtt
3. Hogyan kell alkalmazni a Diphereline SR 3,75
mg injekciót?
4. Lehetséges mellékhatások
5 Hogyan kell a Diphereline SR 3,75 mg
injekciót tárolni?
6 A csomagolás tartalma és egyéb információk
1. Milyen
típusú gyógyszer a Diphereline SR 3,75 mg injekció és milyen betegségek esetén
alkalmazható?
Ez a gyógyszer
egy természetes hormon-analóg.
Alkalmazzák:
Férfiaknál
·
dülmirigy (prosztata)
hormonfüggő karcinómájának (prosztatadaganat) kezelésére (önmagában vagy
radioterápiával egyidejűleg kombinálva).
Nőknél
·
a méhnyálkahártya
rendellenes helyen történő megtapadásának (endometriózis) kezelésére,
·
a méh izomszövetéből eredő
jóindulatú daganat (fibromióma) kezelésére műtét előtt, vagy amikor műtét nem
jön szóba,
·
a meddőség
(infertilitás) bizonyos formáinak kezelésére. Mesterséges megtermékenyítés
(I.V.F.E.T.) esetén a készítményt rendszerint egyéb hormonokkal (úgynevezett gonadotropinokkal)
kombinálva alkalmazzák,
·
hormonkezelésre
reagáló emlődaganat korai stádiumának kezelésére, olyan menopauza előtti
állapotban lévő nőknél, akik korábban kemoterápiában részesültek
A Diphereline SR 3,75 mg injekciót hormontartalmú
gyógyszerekkel együtt alkalmazzák. Lehet, hogy kezelőorvosa az alábbi
készítmény szedését is előírja:
-....... tamofixén nevű gyógyszer - ezt abban
az esetben kapja, ha nagy a daganat kiújulásának a kockázata,
vagy
-....... egy "aromatázgátló"
gyógyszer, mint például az exemesztán - ezt a gyógyszert csak 6‑8 héttel
a Diphereline SR 3,75 mg injekciós kezelés megkezdése után kaphatja.
Ne feledje el gondosan elolvasni a Diphereline SR 3,75
mg injekcióval együtt szedett gyógyszerek betegtájékoztatóját.
Gyermekeknél
·
gyermekeknél korai
pubertás kezelésére.
2. Tudnivalók a Diphereline SR 3,75 mg injekció alkalmazása előtt
Ne alkalmazza
a Diphereline SR 3,75 mg injekciót:
-
ha allergiás
(túlérzékeny) a triptorelinre, a GnRH-ra vagy annak analógjaira, vagy a gyógyszer (6.pontban felsorolt) bármely egyéb
összetevőjére.
-
ha Ön terhes vagy
szoptat.
-
ha emlődaganat miatt
alkalmazza a Diphereline SR 3,75 mg injekciót, csak legalább 6‑8 hétig
tartó Diphereline SR 3,75 mg injekciós kezelést követően alkalmazzon
"aromatázgátló" gyógyszert a Diphereline SR 3,75 mg injekciónel
együtt.
Figyelmeztetések
és óvintézkedések
Egyes esetekben a
Diphereline SR 3,75 mg injekciót alkalmazó betegeknél depresszió kialakulását
jelentették, mely akár súlyos is lehet. Értesítse kezelőorvosát, amennyiben a
Diphereline SR 3,75 mg injekció alkalmazása során depresszív hangulat
alakul ki Önnél. Lehet, hogy kezelőorvosa figyelemmel akarja kísérni az Ön
depresszióját a kezelés során.
Férfiak
Ha Ön véralvadás gátló
szereket használ, az injekció helyén véraláfutást észlelhet.
Kezelés elején szervezetében
megemelkedik a férfi nemi hormon (tesztoszteron) szintje. Ez a daganatos
tünetek rosszabbodásához vezethet. Keresse fel kezelőorvosát, ha ez előfordul.
Kezelőorvosa adhat Önnek egy bizonyos gyógyszert (úgynevezett antiandrogént),
hogy megelőzze ezeknek a tüneteknek a rosszabbodását.
A Diphereline SR 3,75 mg injekciós kezelés első heteiben, mint egyéb GnRH-analóg szerek esetén, egyes
esetekben gerincvelő-összenyomás (kompresszió), vagy húgycső-elzáródás
(vizelési nehézség) léphet fel. Ha ilyen tünetek lépnek fel kezelőorvosa
ellenőrzi, és kezelésben részesíti.
Sebészeti kasztráció után a
triptorelin nem hoz létre további tesztoszteronszint-csökkenést, ezért a here
eltávolítása után nem szabad használni.
A Diphereline SR 3,75 mg
injekciós kezelés alatt vagy a kezelés befejezése után az agyalapi mirigy nemi
funkcióinak diagnosztikus vizsgálatai félrevezetők lehet.
Felnőtteknél, ha a triptorelint
vagy egyéb GnRH-analógot hosszabb ideig alkalmaznak, megnő a vékony vagy gyenge
csontok kialakulásának kockázata, különösen alkoholisták, erős dohányosok
esetében, vagy ha a családi kórelőzményben csontritkulás (olyan állapot, ami a
csontok erősségét befolyásolja) szerepel, nem megfelelő diéta vagy görcsgátló
gyógyszerek szedése (epilepszia vagy görcsrohamok elleni szerek) vagy
kortikoszteroid (szteroidok) alkalmazása esetén. Ha bármilyen kóros eltérése ‑
mint például csontritkulás ‑ van, amely érinti a csontjait,
tájékoztassa kezelőorvosát. Ez befolyásolhatja a kezelőorvosa döntését, hogy milyen
kezelésben részesítse.
Ha Ön cukorbeteg vagy
szívbeteg, tájékoztassa kezelőorvosát.
Ha Ön bármilyen szív-és érrendszeri
betegségben szenved, beleértve a szív ritmuszavarait is (aritmia) vagy ezen
betegségek kezelésére szolgáló gyógyszert szed, tájékoztassa kezelőorvosát. A
Diphereline SR 3,75 mg injekció alkalmazásával a szívritmuszavarok
előfordulásának kockázata emelkedhet.
Ha Önnek agyalapi mirigy‑megnagyobbodása
(jóindulatú daganat) van, melyről nem tudott, ezt felfedezhetik a Diphereline
SR 3,75 mg injekciós kezelés alatt; ennek tünetei közé tartoznak a hirtelen
fejfájás, látászavarok és a szemizmok bénulása.
Nők
Felnőtteknél, ha Diphereline
SR 3,75 mg injekciót vagy egyéb GnRH-analógot analógot hosszabb ideig
alkalmaznak megnő a vékony vagy gyenge csontok kialakulásának kockázata,
különösen alkoholisták, erős dohányosok esetében, vagy ha a családi kórelőzményben
csontritkulás (olyan állapot, ami a csontok erősségét befolyásolja) szerepel,
nem megfelelő diéta vagy görcsgátló gyógyszerek szedése (epilepszia vagy görcsrohamok
elleni szerek) vagy kortikoszteroid (szteroidok) alkalmazása esetén. Ha
bármilyen kóros eltérése ‑ mint például csontritkulás ‑ van,
amely érinti a csontjait, tájékoztassa kezelőorvosát. Ez befolyásolhatja a
kezelőorvosa döntését, hogy milyen kezelésben részesítse.
A
kezelés első hónapjában hüvelyi vérzése lehet azután, hogy a havi vérzése
normálisan megszűnt. Tájékoztassa kezelőorvosát, ha a kezelés első hónapja után
vérzése van.
Havi
vérzése 2-3 hónappal az utolsó injekció után fog kezdődni. A kezelés első
hónapjában és az utolsó injekció után a fogamzásgátlás valamilyen módszerét (nem
fogamzásgátló tablettát) kell alkalmazni, ha a kezelést nem a meddőség ellen
alkalmazták.
Ha Ön emlődaganat kezelésére
kapja a Diphereline SR 3,75 mg injekciót
Ha Önnek bármilyen kóros
eltérése ‑ mint például csontritkulás (oszteoporózis) ‑ van,
amely érinti a csontjait, tájékoztassa kezelőorvosát. Ez befolyásolhatja orvosa döntését az Ön kezelésére
vonatkozóan. Kezelőorvosa csontsűrűség‑vizsgálatot fog végeztetni a
kezelés megkezdése előtt, ha Önnél fennáll az oszteoporózis kockázata, és a
kezelés ideje alatt megfigyelés alatt fogja tartani Önt.
Ha Önnek
cukorbetegsége (dibetésze) vagy magas vérnyomása van, tákékoztassa erről
kezelőorvosát. Orvosa ellenőrizni fogja az Ön vércukorszintjét és vérnyomását a
kezelés ideje alatt.
Ha Ön
depresszióban szenved, tájékoztassa erről kezelőorvosát. Lehet, hogy kezelőorvosa
figyelemmel akarja kísérni az Ön depresszióját a kezelés során.
Gyermekek
és serdülők
A
korai pubertásban szenvedő leányoknál a kezelés első hónapjában hüvelyi vérzés
léphet fel.
Amennyiben
növekvő agydaganata van, kérjük, tájékoztassa kezelőorvosát.
Ha
a fenti tünetek bármelyike miatt aggódik, forduljon kezelőorvosához.
Egyéb
gyógyszerek és a Diphereline SR 3,75 mg injekció
Feltétlenül tájékoztassa
kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint
alkalmazni tervezett egyéb gyógyszereiről, beleértve a vény nélkül kapható
készítményeket is.
Férfiak
A Diphereline SR 3,75 mg
injekció kölcsönhatásba léphet egyéb szívritmuszavarok kezelésére alkalmazott
gyógyszerekkel (például kinidin, prokainamid, amiodaron és szotalol), vagy
megnövelheti a szívritmuszavarok előfordulásának kockázatát, ha egyéb
gyógyszerekkel, például metadonnal (fájdalomcsillapításra és gyógyszerfüggőség
esetén a méregtelenítés részeként alkalmazzák), moxifloxacinnal (egy
antibiotikum), antipszichotikumokkal (súlyos elmebetegségben alkalmazott
gyógyszerek) együtt alkalmazzák.
Terhesség
és szoptatás
A Diphereline SR 3,75 mg
injekció nem alkalmazható terhesség vagy szoptatás idején.
Ne alkalmazza a Diphereline SR 3,75 mg injekciót, ha terhességet tervez (kivéve, ha a Diphereline SR 3,75 mg injekció a meddőségi kezelés része).
A
készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges
képességekre
Szédülést, fáradtságot vagy
látászavarokat, mint a homályos látás, érezhet. Ezek lehetnek az injekciós
kezelés mellékhatásai vagy az alapbetegsége következményei. Ha Ön bármelyik
fenti mellékhatást tapasztalja, ne vezessen gépkocsit, és ne használjon
munkagépeket.
A
Diphereline SR 3,75 mg injekció nátriumot tartalmaz
A
készítmény kevesebb mint 1 mmol (23 mg) nátriumot tartalmaz injekciós
üvegenként, azaz gyakorlatilag nátriummentes.
3. Hogyan kell alkalmazni a Diphereline SR 3,75
mg injekciót?
A
Diphereline SR 3,75 mg injekciót kezelőorvosa vagy a gondozását végző
egészségügyi szakember fogja Önnek izomba (intramuszkulárisan) beadni.
Az
injekció előkészítésére vonatkozó információkat lásd a betegtájékoztató végén.
Az
elkészült oldat egyéb gyógyszerekkel nem keverhető.
Prosztatakarcinóma, endometriózis,
fibromióma, illetve meddőség kezelése
Az ajánlott adag 4 hetente (28 naponta) 1 db izomba adott (intramuszkuláris)
injekció.
Emlődaganat
kezelése
Az
ajánlott adag 4 hetente (28 naponta)
egy izomba adott (intramuszkuláris) injekció. A kezelés akár 5 évig is
eltarthat.
A
Diphereline SR 3,75 mg injekciót általában egy "tamoxifén" nevű
gyógyszerrel vagy egy "aromatázgátlóval", például
"exemesztánnal" együtt alkalmazzák.
Ha
aromatázgátló gyógyszert kell kapnia, annak megkezdése előtt legalább 6‑8 hetes
Diphereline SR 3,75 mg injekciós kezelésben kell részesülnie. Legalább két Diphereline SR 3,75 mg injekciót meg kell
kapnia (a 2 injekció között 4 hétnek kell eltelnie) az aromatázgátló-kezelés
megkezdése előtt.
Alkalmazása
gyermekeknél
Az
adagot a testsúlynak megfelelően kell kiszámolni.
30 kg feletti testsúlyú gyermekek: 4 hetente (28 naponta) 1 db izomba adott
(intramuszkuláris) injekció
20-30 kg testsúlyú gyermekek: 4 hetente (28 naponta) a dózis kétharmadát kell
izomba (intramuszkulárisan) beadni, tehát az 1 db injekció feloldása után
elkészült oldat kétharmadát kell alkalmazni.
20 kg testsúly alatti gyermekek: 4 hetente (28 naponta) a dózis felét kell izomba
(intramuszkulárisan) beadni, tehát az 1 db injekció feloldása után
elkészült oldat felét kell alkalmazni.
Ha
abbahagyja a Diphereline SR 3,75 mg injekció alkalmazását
Ne
szakítsa meg a Diphereline SR 3,75 mg injekciós kezelést anélkül, hogy ezt
előtte kezelőorvosával megbeszélné. Ez különösen fontos akkor, ha Ön
egyidejűleg egy aromatázgátló gyógyszert is szed, mivel ez esetben a kezelés
megszakítása az ösztrogénszint emelkedését okozhatja. Kezelőorvosa rendszeresen
ellenőrizni fogja az Ön ösztrogénszintjét a Diphereline SR 3,75 mg injekciós
kezelés alatt.
Ha
Ön abbahagyja a Diphereline SR 3,75 mg injekció alkalmazását, 1 hónapon belül
abba kell hagynia az aromatázgátló gyógyszer alkalmazását is.
Ha bármilyen további kérdése
van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát.
4. Lehetséges mellékhatások
Mint
minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek
azonban nem mindenkinél jelentkeznek.
Ritkán súlyos allergiás
reakciók léphetnek fel. Azonnal szóljon kezelőorvosának, ha nyelési vagy
légzési problémák, az ajkak, arc, torok vagy nyelv megduzzadása, vagy kiütések
léptek fel.
A gyógyszer hosszú idejű
alkalmazásas felnőtteknél a csontállomány csökkenéséhez vezethet.
Ha Önnek agyalapi mirigy
megnagyobbodása (jóindulatú daganat) van, de erről nem tudott, ezt
felfedezhetik a Diphereline SR 3,75 mg injekciós kezelés alatt; ennek
tünetei hirtelen fejfájás, látászavarok, szemizmok bénulása lehet
A Diphereline SR 3,75 mg injekciós, mint más GnRH
analóggal történt kezelés során a fehérvérsejtszám emelkedése léphet fel.
Mellékhatások férfi
betegeknél
A várható mellékhatások legtöbbje
a szervezetben fellépő tesztoszteronszint (férfi nemi hormon) változás
következménye. Ilyen hatások többek között a hőhullámok, impotencia és csökkent
libidó.
Nagyon gyakori
mellékhatások: 10-ből több mint 1
beteget érinthet
·
Hőhullámok
·
Gyengeség
·
Fokozott verítékezés
·
Hátfájás
·
Fonákérzés/zsibbadás a lábakban
·
Csökkent nemi vágy (libidó)
·
Merevedési zavar (impotencia,
ejakulációs zavar, ill. rendellenesség)
Gyakori mellékhatások: 100-ből 1-10 beteget érinthet
·
Hányinger, szájszárazság
·
Fájdalom, bevérzés, kivörösödés és
duzzanat az injekció beadásakor, izom és csontfájdalmak, fájdalom a karokban és
lábakban, vizenyő (ödéma: folyadék-visszatartás a test szöveteiben),
kismedencei fájdalom
·
Allergiás reakció
·
Testsúlynövekedés
·
Szédülés, fejfájás
·
Nemi vágy (libidó) megszűnése, depresszió,
hangulatváltozások
·
Magas vérnyomás
Nem gyakori mellékhatások:
1000-ből 1-10 beteget
érinthet
·
A vérlemezkék számának csökkenése,
mely növeli a vérzések, véraláfutások kockázatát
·
Szívdobogásérzés
·
Fülcsengés, forgó jellegű
szédülés, homályos látás
·
Hasi fájdalom, székrekedés,
hasmenés, hányás
·
Álmosság, remegés, aluszékonyság, fájdalom
·
Egyes laboratóriumi vizsgálatok
eredményei változhatnak (emelkedett májfunkciós értékek)
·
Vérnyomás-emelkedés
·
Testsúlycsökkenés
·
Étvágytalanság, fokozott étvágy,
köszvény (súlyos fájdalom és duzzanat az izületekben, rendszerint a
nagylábujjban), cukorbetegség (diabétesz), a vérzsírok szintjének jelentős
emelkedése
·
Ízületi fájdalmak, izomgörcs,
izomgyengeség, izomfájdalmak, boka-, láb- vagy az ujjak duzzanata,
csontfájdalom
·
Bizsergés vagy zsibbadás
·
Alvási képtelenség, ingerlékenység
(irritábilitás)
·
Az emlők megnagyobbodása
férfiaknál, mellfájdalom, a herék méretének csökkenése, herefájdalom
·
Légzési nehézségek
·
Pattanások (akné), hajhullás,
viszketés, bőrkiütés, bőrvörösség, csalánkiütés
·
Éjszakai vizelés, vizeletürítési
nehézségek
·
Orrvérzés
Ritka mellékhatások: 10 000-ből 1-10 beteget érinthet
·
A bőr vöröses, lilás elszíneződése
·
Kóros érzékelés a szemben,
látászavarok,
·
Hasi teltségérzet, puffadás, kórós
ízérzékelés
·
Mellkasi fájdalom
·
Állási nehézség
·
Influenzaszerű tünetek, láz
·
Súlyos allergiás reakció, ami
szédülést, nehézlégzést, arc-és nyelvduzzanatot okozhat
·
Orr-/torokgyulladás
·
Ízületi merevség, ízületi duzzanat,
mozgásszervi merevség, csontízületi gyulladás (oszteoartritisz)
·
Feledékenység
·
Zavartság, csökkent aktivitás,
emelkedett kedélyállapot
·
Légszomj, mely vízszintes
fekvéskor kifejezett
·
Hólyagok a bőrön
·
Alacsony vérnyomás
A forgalomba hozatalt
követően az alábbi mellékhatásokról is beszámoltak: anafilaxiás reakció (súlyos
allergiás reakció. mely nehézlégzést vagy szédülést okoz), EKG-eltérés (QT‑megnyúlás),
általános rossz közérzet, szorongás, valamint csalánkiütés gyors kialakulása a
bőr vagy a nyálkahártyák duzzanata miatt, vizelet-visszatartási képtelenség
(inkontinencia).
Mellékhatások
nőbetegeknél:
A várható mellékhatások
többsége a szervezetben fellépő ösztrogénszint-változás következménye.
Az ezek közé tartozó nagyon
gyakori (10-ből több mint 1
beteget érinthet) mellékhatások:
fejfájás, csökkent nemi vágy, hullámzó kedélyállapot, alvási nehézségek, emlőbetegségek,
fájdalom a nemi közösülés alatt vagy azt
követően, nemiszervek vérzése, petefészek-túlműködési
tünetegyüttes (ovárium hiperstimulációs szindróma), petefészek-megnagyobbodás, medencefájdalom,
hüvelyszárazság, fokozott izzadás, pattanások (akné), olajos bőr, hőhullámok és
gyengeség.
Gyakori mellékhatások
(100-ből 1-10 beteget érinthet),
amelyek felléphetnek: emlőfájdalom, izomgörcsök, ízületi fájdalom,
testsúlynövekedés, hányinger, depresszió, idegesség, hasi fájdalom vagy
diszkomfort, fájdalom, véraláfutás, bőrpír és duzzanat az injekció beadási
helyén, boka-, láb- vagy az ujjak duzzanata, allergiás reakció, fájdalom a
karokban és a lábakban, szédülés.
Nem gyakori (1000-ből 1-10 beteget érinthet) mellékhatások:
szívdobogásérzés, forgó jellegű szédülés, szemszárazság, homályos látás,
puffadás, hányás, szájszárazság, felfúvódás, szájfekély, testtömeg-csökkenés,
az étvágy csökkenése, vízvisszatartás, hátfájás, izomfájdalom, megváltozott
ízérzés, érzéketlenség, átmeneti eszméletvesztés, emlékezetkiesés, koncentráció
hiánya, bizsergés vagy zsibbadás, akaratlan izommozgás, hangulatváltozás,
szorongás, zavartság, vérzés közösülés után, hólyagsérv, szabálytalan
időszakokban bekövetkező vagy fájdalmas illetve erős havi vérzés (menstruáció),
kis ciszták (folyadékkal teli hólyagok) kialakulása a petefészekben, amelyek
fájdalmat okozhatnak, hüvelyi folyás, nehézlégzés, orrvérzés, hajhullás, száraz
bőr, túlzott szőrnövekedés, törékeny körmök, viszketés, bőrkiütés.
A forgalomba hozatalt
követően az alábbi mellékhatásokról is beszámoltak (gyakoriságuk a rendelkezésre álló adatok
alapján nem becsülhető meg): láz, általános
rossz közérzet, magas vérnyomás, súlyos allergiás, mely nehézlégzést vagy
szédülést okoz, arc- vagy torokduzzanat, néhány laboratóriumi vizsgálati érték
változása (beleértve a májfunkciós értékek emelkedését is), izomgyengeség,
zavartság, a menstruációs ciklusok kimaradása, csalánkiütés gyors kialakulása a
bőr vagy a nyálkahártyák duzzanata következtében, kórós érzékelés a
szemben/vagy a látás megváltozás, hasmenés.
A gonadotropinokkal kombinált
meddőség elleni kezelés a petefészkek méretének növekedését vagy
petefészek-túlműködést okozhat, mely medence- és/vagy hasi fájdalmakat vagy
légszomjat okozhat. Ha ezek fellépnek, keresse fel kezelőorvosát, amint
lehetséges.
Az
endometriózis kezelésekor, a kezelés kezdetén felerősödhetnek a kezelést indokló
panaszok (kismedencei fájdalom, a havi vérzés rendellenességei, ún.
diszmenorrea), de ennek egy-két hét alatt el kell múlnia. Ez még akkor is
bekövetkezhet, ha a kezelés kedvező hatást fejt ki. Mindenesetre haladéktalanul
értesítse orvosát, ha ilyen jelenséget észlel.
Emlődaganat tamoxifénnel
vagy aromatázgátlóval történő kombinációs kezelésekor észlelt mellékhatások
Az alábbi mellékhatásokat észlelték,
amikor a Diphereline SR 3,75 mg
injekciót emlődaganat kezelésére, akár tamoxifénnel,
akár aromatázgátlóval kombinációban alkalmazták:
Nagyon gyakori
mellékhatások (10-ből több mint 1
beteget érinthet): hányinger, nagyfokú
fáradtságérzet, izületi- és izomájdalom, csontritkulás (oszteoporózis), hőhullámok,
fokozott izzadás, alvászavarok, depresszió, csökkent nemi vágy (libidó),
hüvelyszárazság, fájdalom a nemi közösülés alatt vagy azt követően, vizelet-visszatartási
nehézség (inkontinencia), vérnyomás-emelkedés.
Gyakori mellékhatások (100-ből 1-10 beteget érinthet): cukorbetegség, magas vércukorszint (hiperglikémia),
fájdalom, véraláfutás, bőrpír és duzzanat az injekció beadásának helyén, allergiás
reakció, csonttörések, vérrög az erekben.
Nem gyakori mellékhatások
(1000-ből 1-10 beteget
érinthet): agyvérzés, az agy
vagy a szív vérellátásának hiánya.
Ritka mellékhatások (10 000-ből
1-10 beteget érinthet): EKG‑eltérések
(QT-megnyúlás)
Mellékhatások gyermekeknél
Nagyon gyakori (10-ből
több mint 1 beteget érinthet) mellékhatások:
lányoknál a kezelés első hónapjában hüvelyi eredetű vérzés léphet fel.
Gyakori (100-ből
1-10 beteget érinthet) mellékhatások:
hasi fájdalom, fájdalmas véraláfutás, bőrpír és duzzanat az injekció beadási
helyén, fejfájás, hőhullámok, testsúlynövekedés, pattanások (akné),
túlérzékenységi reakciók.
Nem gyakori (1000-ből
1-10 beteget érinthet) mellékhatások:
homályos látás, hányás, székrekedés, hányinger, általános rossz közérzet,
túlsúlyosság, nyaki fájdalom, hangulatváltozások, emlőfájdalom, orrvérzés,
viszketés, kiütés vagy csalánkiütés a bőrön.
A forgalomba hozatalt
követően az alábbi mellékhatásokról is beszámoltak (gyakoriságuk a rendelkezésre álló adatok
alapján nem becsülhető meg) :magas
vérnyomás, látászavarok, súlyos allergiás reakció, mely nehézlégzést vagy
szédülést és arc- vagy torokduzzanatot okoz felnőtt férfiakon és nőkön, néhány
laboratóriumi vizsgálati érték változása (beleértve a hormonszinteket is), csalánkiütés
gyors kialakulása a bőr vagy a nyálkahártyák duzzanata következtében,
izomfájdalom, hangulatzavarok, depresszió, idegesség.
A
mellékhatások jelentése
Ha
Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét.
Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is
vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V.
függelékben található elérhetőségeken keresztül.
A
mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több
információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával
kapcsolatban.
5. Hogyan kell a Diphereline SR
3,75 mg injekciót tárolni?
A
gyógyszer gyermekektől elzárva tartandó!
Ez a gyógyszer nem igényel
különleges tárolást.
Az elkészített
szuszpenziót azonnal fel kell használni.
A csomagoláson
feltüntetett lejárati idő (Felhasználható:) után ne alkalmazza ezt a
gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Ne
alkalmazza a készítményt, ha a csomagoláson bármilyen rongálódást észlel.
Semmilyen gyógyszert ne dobjon a
szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit
tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a
környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a
Diphereline SR 3,75 mg injekció?
-
A készítmény hatóanyaga: Egy port tartalmazó injekciós üveg 4,20 mg
triptorelint (triptorelin‑acetát formájában) tartalmaz.
Az
injekciós üveg rámérést tartalmaz a hatóanyagból annak érdekében, hogy a
minimális hatásos mennyiség bejusson a beteg szervezetébe.
-
Egyéb összetevők:
Port
tartalmazó injekciós üveg: D,L-laktid-koglikolid-polimer,
poliszorbát 80, karmellóz‑nátrium, mannit, nitrogén
Oldószerampulla:
mannit, injekcióhoz való víz
Milyen a készítmény
külleme és mit tartalmaz a csomagolás?
Küllem:
Por: kb. 312 mg, gyakorlatilag fehér, steril, laza,
liofilizátum.
Oldószer: kb. 2 ml tiszta, színtelen, steril, vizes
oldat.
Csomagolás:
Port tartalmazó injekciós
üveg: rollnizott gumidugóval lezárt,
halványan színezett, átlátszó, injekciós üveg.
Oldószer ampulla: színtelen, átlátszó üvegampulla.
Steril
buborékcsomagolás, amely tartalmaz egy steril, egyszer használatos PP
fecskendőt, és két steril, egyszer használatos tűt.
1 buborékcsomagolás + 1 port
tartalmazó injekciós üveg + 1 oldószer ampulla dobozban.
A forgalomba hozatali
engedély jogosultja:
Ipsen Pharma
65 Quai Georges Gorse
92100 Boulogne Billancourt
Franciaország
Gyártó:
Ipsen Pharma Biotech
83870 Signes, Franciaország
A készítményhez kapcsolódó
további kérdéseivel forduljon a forgalomba hozatali engedély jogosultjának
helyi képviseletéhez:
Ipsen Pharma SAS
Magyarországi Kereskedelmi Képviselet
1133 Budapest, Árbóc u. 6.
Tel.: +36-1/555-5930
Fax: +36-1/555-5949
OGYI-T-8169/01
A
betegtájékoztató legutóbbi felülvizsgálatának dátuma: 2017. április
Az alábbi információk
kizárólag egészségügyi szakembereknek szólnak:
AZ INJEKCIÓ ELKÉSZÍTÉSÉRE
VONATKOZÓ ÚTMUTATÓ
|
1 - A BETEG ELŐKÉSZÍTÉSE
AZ INJEKCIÓ ELKÉSZÍTÉSE ELŐTT
|
|
Készítse elő a beteget,
fertőtlenítse a gluteális izmot az injekció beadási helyénél. Ezt a műveletet
feltétlenül az injekció elkészítése előtt végezze el, mivel a feloldást
követően az elkészült injekciót azonnal be kell adni.
|
|
2 – AZ INJEKCIÓ
ELKÉSZÍTÉSE
|
|
|
Két tű található a dobozban:
• Egyes tű (Needle 1) : egy 20G jelű ( 38 mm hosszú), biztonsági
védőeszköz nélküli, a szuszpendáláshoz használandó tű
• Kettes tű (Needle 2) : egy 20G jelű ( 38 mm hosszú), biztonsági
védőeszközzel rendelkező , az injekció beadásához használandó tű

Buborékok jelenléte a
liofilizátum tetején normál jelenség a készítménynél.
|
|
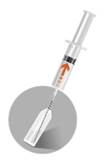
2a
o
Vegye ki az oldószert tartalmazó
ampullát. Gyengéden rázza le az ampulla felső részéből a folyadékot az
ampulla testébe.
o
Csavarja rá az egyes tűt (Needle
1, biztonsági védőeszköz
nélkül) a fecskendőre. Még ne távolítsa
el a tűvédő tokot.
o
Törje le az oldószerampulla
nyakát úgy, hogy a törőpont szemben legyen.
o
Távolítsa el a tű védőborítását
az egyes tűről. Helyezze a tűt az ampullába és szívja fel az összes oldószert
a fecskendőbe. Tegye félre az oldószert tartalmazó fecskendőt.
|
|
|
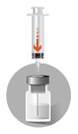
2b
o
Vegye ki a port tartalmazó
injekciós üveget. Gyengéden rázza le az injekciós üveg tetején összegyűlt
port az injekciós üveg aljába.
o
Távolítsa el az injekciós üveg
tetején található műanyag zárólapot.
o
Vegye kézbe újra az oldószert
tartalmazó fecskendőt, és szúrja át a tűt függőlegesen a gumidugón az
injekciós üvegbe. Olyan lassan fecskendezze az oldószert a porampullába,
amilyen lassan csak lehet, hogy lemossa a porampulla teljes felső részét.
|
|
|
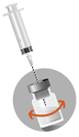
2c
o
Húzza az egyes tűt a folyadék
szintje fölé. Ne húzza ki a tűt az üvegből. Forgassa a porampullát egyik
oldaláról a másikra a szuszpenzió kialakulásáig. Ne fordítsa fel a
porampullát.
o
Győződjön meg róla, hogy a
mozgatás elegendő volt ahhoz, hogy homogén, tejszerű szuszpenzió jöjjön
létre.
o
Fontos: Ellenőrizze, hogy
nincs-e szuszpendálatlan por az injekciós üvegben (ha csomók van jelen, addig
folytassa a rázogatást, amíg el nem tűnnek)
|
|
|
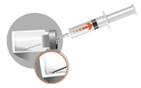
2d
o
Amikor a szuszpenzió homogén,
nyomja le a tűt az üveg aljáig, és az injekciós üveg megfordítása nélkül
szívja ki az összes szuszpenziót. Egy kis mennyiség az injekciós üvegben fog
maradni, ezt meg kell semmisíteni. A felültöltés miatt ez a veszteség
megengedhető.
|
|
|
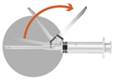
o
A tű levételéhez fogja meg a
színes részt. Távolítsa el a felszíváshoz használt egyes tűt a fecskendőről. Csavarja rá a
fecskendőre a kettes, biztonsági védőeszközzel rendelkező tűt.
o
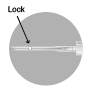
Mozdítsa a biztonsági tokot
a tűtől a fecskendő felé. A biztonsági tok az
Ön által beállított pozícióban marad.
o
Távolítsa el a tűvédőt a tűről.
o
Nyomja ki a levegőt a
fecskendőből közvetlenül az injekció beadása előtt.
|
|
|
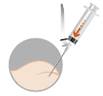
3 – INTRAMUSZKULÁRIS INJEKCIÓ BEADÁSA
|
|
- A kicsapódás elkerülése
érdekében azonnal adja be az injekciót az előzőleg fertőtlenített
farizomba.
|
|
|
4 – HASZNÁLAT UTÁN
|
|
|
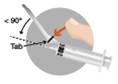
o
Egykezes technikával aktiválja a
biztonsági védőrendszert
o
Megjegyzés: tartsa ujját
mindenkor a védőeszköz (Tab) mögött.
Kétféle
módszer van a biztonsági rendszer aktiválására:
o
"A" módszer: ujjával
nyomja előre a védőeszközt
o
"B" módszer: nyomja a
védőeszközt egy sima felületre
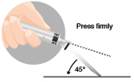
o
Mindkét esetben határozott,
gyors mozdulattal nyomja le a védőt, amíg egy különálló hallható kattanást nem hall.
o
Vizuálisan ellenőrizze, hogy a
tű teljes mértékben be van zárva.
A használt injekciós tűket,
a megmaradt szuszpenziót vagy egyéb hulladékot a gyógyszerekre vonatkozó
előírásoknak megfelelően kell megsemmisíteni.
|
vagy
|









